
【题目】在体积不变的密闭容器中,保持一定的温度发生下列反应:4A(g)+B(?)2C(g)+2D(g),请用“增大”“减小”“不变”或“能”“不能”填空。
(1)当B为固体时,若反应向右进行,容器内混合气体的密度___________;若反应向左进行,容器内混合气体的密度___________;当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(2)当B为气体时,不论向哪个方向反应,容器内混合气体的密度___________,故当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(3)当B为固体时,无论向哪个方向反应,容器内混合气体的压强___________,故当容器内混合气体的压强不变时___________说明反应已经达到平衡。
【答案】增大 减小 能 不变 不能 不变 不能
【解析】
当B为固体时,若反应向右进行,容器内混合气体的密度ρ=![]() 进行分析密度的变化,根据变量不变可以作为判断平衡的标志;在体积不变的密闭容器中,B为气体时,根据ρ=
进行分析密度的变化,根据变量不变可以作为判断平衡的标志;在体积不变的密闭容器中,B为气体时,根据ρ=![]() 分析密度的变化。
分析密度的变化。
(1)当B为固体,若反应向右进行,由方程式可知,容器中混合气体的总质量随反应的进行而增大;由于容器体积不变,并且密闭,说明气体体积不变,由ρ=![]() 可知,混合气体的密度增大;若反应向左进行,则气体的质量随反应的进行而减小,气体体积不变,则密度减小;当容器内混合气体的密度不变时,说明容器中混合气体的总质量不变,平衡不移动,说明反应已经达到平衡;
可知,混合气体的密度增大;若反应向左进行,则气体的质量随反应的进行而减小,气体体积不变,则密度减小;当容器内混合气体的密度不变时,说明容器中混合气体的总质量不变,平衡不移动,说明反应已经达到平衡;
(2) 当B为气体时,根据质量守恒可知,反应前后气体的总质量不变。反应在体积不变的密闭容器中进行,由ρ=![]() 可知,不论向哪个方向反应,容器内混合气体的密度都不变;故当容器内混合气体的密度不变时,不能说明反应已经达到平衡;
可知,不论向哪个方向反应,容器内混合气体的密度都不变;故当容器内混合气体的密度不变时,不能说明反应已经达到平衡;
(3)当B为固体时,由反应方程式可知,气体的物质的量不发生变化,由于体积不变,所以不论向哪个方向反应,容器内混合气体的压强都不变;故当容器内混合气体的压强不变时,不能说明反应已经达到平衡。


科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+B![]() C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
A.若B是气体,增大A的浓度会使B的转化率增大
B.若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
C.升高温度,C质量分数减少,说明正反应为放热反应
D.增大压强,平衡不移动,说明B、D一定是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,下列叙述正确的是![]()
A.![]() 的
的![]() 与
与![]() 混合溶液中
混合溶液中![]()
B.![]() 的可乐中
的可乐中![]() 是
是![]() 的柠檬水中
的柠檬水中![]() 的10倍
的10倍
C.AgCl在![]()
![]() 溶液和
溶液和![]() NaCl溶液中的溶解度相同
NaCl溶液中的溶解度相同
D.![]() 溶液加水稀释至100mL,pH和
溶液加水稀释至100mL,pH和![]() 均减小
均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯是一种难溶于水,密度大于水的无色油状液体,具有茉莉花气味,可用做调香剂。
(一)以乙烯,甲苯为原料,合成乙苯甲酯的路线如图所示。

(1)写出由乙烯制备A的化学方程式______。
(2)写出生成乙酸苯甲酯的化学方程式______。
(3)C到苯甲醇的反应类型______。
(二)制备乙酸苯甲酯的流程如图:
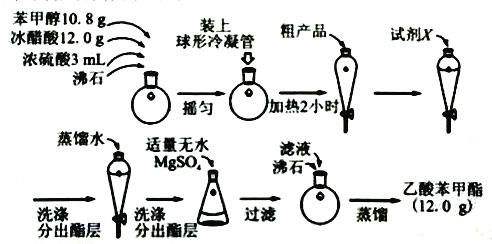
(4)球形冷凝管的作用为______。
(5)试剂X可为______。
A.氢氧化钠溶液 B.碳酸钠溶液 C.乙醇 D.氯化钠溶液
(6)分出酯层时应收集______层液体(填“上”或“下”)
(7)无水MgSO4的作用为______。
(8)本实验所得乙酸苯甲酯的产率为______。(已知:相对分子量:苯甲醇:108;乙酸:60;乙酸苯甲酯:150)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某三元羧酸H3A在表面活性剂、洗涤剂、润滑剂等方面具有重要的地位。常温时,向10mL0.01mol·L-1的H3A溶液中滴入0.01mol·L-1的NaOH溶液,H3A、H2A-、HA2-、A3-的物质的量分数与溶液的pH的关系如图所示。则下列说法中错误的是( )

A.常温时,0.01mol·L-1的H3A溶液的pH介于2~3之间
B.常温时,反应A3-+H2O ![]() HA2-+OH-的平衡常数为K=10c-14
HA2-+OH-的平衡常数为K=10c-14
C.若b=7,则将等物质的量的NaH2A与Na2HA加入到适量蒸馏水中使其完全溶解,则所得的溶液的pH一定等于7
D.加入NaOH溶液的体积为30mL时,所得溶液中存在有:c(OH-)=3c(H3A)+2c(H2A-)+c(HA2-)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业上以制作印刷电路的废液![]() 含
含![]() 、
、![]() 、
、![]() 、
、![]() 生产CuCl的流程:
生产CuCl的流程:
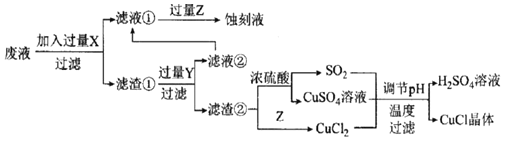
已知:CuCl是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化为绿色,见光分解变成褐色。
请回答下列问题:
(1)流程中的滤渣①与Y反应和X与Y反应相比,单位时间内得到的气体多,其原因为______。
(2)滤液②需要加过量Z,检验Z过量的方法是______。
(3)写出生成CuCl的离子方程式:______。
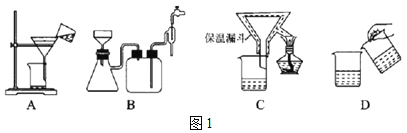
(4)为了提高CuCl产品的纯度,流程中的“过滤”操作适宜用下列装置![]() 图
图![]() 中的______
中的______![]() 填选项字母
填选项字母![]() ,过滤后,洗涤CuCl的试剂宜选用______
,过滤后,洗涤CuCl的试剂宜选用______![]() 填“无水乙醇”或“稀硫酸”
填“无水乙醇”或“稀硫酸”![]()
![]() 加入饱和NaCl溶液中会部分溶解生成
加入饱和NaCl溶液中会部分溶解生成![]() ,在一定温度下建立两个平衡:
,在一定温度下建立两个平衡:
I.CuCl![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。
(5)分析![]() 、
、![]() 和
和![]() 、K的数学关系,在图2中画出
、K的数学关系,在图2中画出![]() 、
、![]() 的关系曲线________(要求至少标出一个坐标点)
的关系曲线________(要求至少标出一个坐标点)
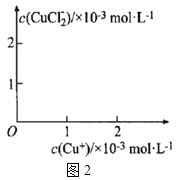
(6)氯化亚铜的定量分析:
①称取样品![]() 于250mL锥形瓶中,加入10mL过量的
于250mL锥形瓶中,加入10mL过量的![]() 溶液,不断摇动:
溶液,不断摇动:
②待样品溶解后,加入20mL蒸馏水和2滴指示剂;
③立即用![]() 硫酸铈标准溶液滴定至绿色为终点;
硫酸铈标准溶液滴定至绿色为终点;
④重复三次,消耗硫酸铈溶液的平均体积为![]() 。
。
上述相应化学反应为![]() 、
、![]() ,则样品中CuCl的纯度为______
,则样品中CuCl的纯度为______![]() 保留三位有效数字
保留三位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、NO、NO2、SO2等有毒气体会危害人体健康,破坏环境,对其进行无害处理研究一直是科技界关注的重点。请回答以下问题:
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.3kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=+179.5kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式__。
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,若反应达到平衡时,所得的混合气体中含N2的体积分数随
N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,若反应达到平衡时,所得的混合气体中含N2的体积分数随![]() 的变化曲线如图1。
的变化曲线如图1。

①a、b、c、d四点的平衡常数从大到小的顺序为__。
②若![]() =0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为__。
=0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为__。
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极的电极反应式为__,经过一段时间后,若乙中需加0.1molCu2(OH)2CO3可使溶液复原,则转移的电子数为__NA。
(4)常温下,SO2可以用碱溶液吸收处理。若将SO2通入到NaOH溶液中,充分反应后得到amol·L-1的NaHSO3溶液,该溶液的pH=5,则该溶液中c(SO32-)___c(H2SO3)(填“>”、“=”或“<”),HSO3-的电离常数约为___(用含a的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】"绿色化学"的理想状态是反应物的原子全部转化为目标产物。以下反应不符合绿色化学原则的是
A.工业生产环氧乙烷:2CH2=CH2+O2![]()
![]()
B.水煤气合成甲醇:CO+ 2H2 ![]() CH3OH
CH3OH
C.铝热反应:2Al+ Fe2O3![]() 2Fe + Al2O3
2Fe + Al2O3
D.合成甲基丙烯酸甲酯:![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为: N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1,
I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应;
(1)测得反应放出的热量_____92.4kJ (填“小于”,“大于”或“等于”)
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_____。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_______(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将__________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度______(填“大于”、“小于”或“等于”)原来的2倍。
II.该反应N2(g)+3H2(g)2NH3(g) △H=﹣92.4kJ/mol 在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。
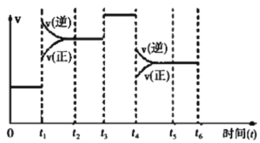
(1)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
t1__________,t3__________,t4__________。
(2)下列时间段中,氨的百分含量最高的是_______
A.0~t1B.t2~t3 C.t3~t4D.t4~t5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com