
【题目】用0.1molL﹣1的盐酸滴定25.00mLNa2CO3溶液,其滴定曲线如图所示,下列说法正确的是( ) 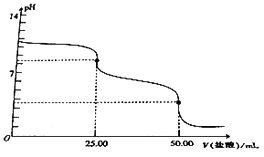
A.Na2CO3溶液的浓度为0.2molL﹣1
B.当V(盐酸)=0时,溶液中:c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3)
C.当V(盐酸)=25.00mL时,溶液中:c(Cl﹣)>c(HCO3﹣)>c(CO32﹣)>c(H2CO3)
D.当V(盐酸)=50.00mL时,溶液中:c(Na+)+c(H+)=c(OH﹣)+c(Cl﹣)
【答案】B
【解析】解:A.用0.1molL﹣1的盐酸滴定25.00mLNa2CO3溶液,当消耗V(HCl)=25.00mL时,溶液的pH发生急剧变化,说明此时二者恰好完全反应,二者物质的量以1:1反应,二者的体积相,则浓度相等,所以碳酸钠溶液浓度为0.1mol/L,故A错误;B.当盐酸体积为0时,溶液中溶质为碳酸钠,存在质子守恒,根据质子守恒得c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3),故B正确;
C.当V(盐酸)=25.00mL时,溶液中溶质为等物质的量浓度的碳酸氢钠和氯化钠,碳酸氢根离子水解导致溶液呈碱性,但其水解程度较小,其水解程度大于电离程度,所以c(CO32﹣)<c(H2CO3),故C错误;
D.当V(盐酸)=50.00mL时,二者恰好完全反应生成氯化铵、碳酸,溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH﹣)+c(Cl﹣)+(HCO3﹣)+2c(CO32﹣),故D错误;
故选B.


 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】氮及其化合物在生产、生活中有着重要的作用.请回答下列问题: 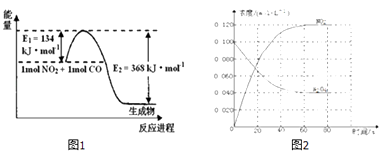
(1)图1是常温下1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(2)在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)2NO2(g)△H如图2
①在0﹣60s时段,反应速率v(N2O4)为molL﹣1s﹣1 .
②温度升高,混合气体的颜色变深,则△H0(填“>”或“<”).
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有(填字母).
a.向混合气体中通入N2O4 b.升高温度
c.向混合气体中通入NO2 d.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2 , 反应2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1的CH3COONa溶液.
①A、B两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为(已知HNO2的电离
常数Ka=7.1×10﹣4molL﹣1 , CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1).
②可使A、B两溶液的PH相等的方法是(填字母).
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(4)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平).0.6molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,我国女药学家屠呦呦因发现了青蒿素( C15H22Os)而获得诺贝尔奖,青蒿素的一种化学合成路线如图: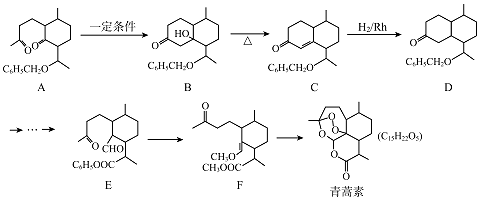
(1)化合物D的分子式为 , D中含有的官能团名称是 .
(2)合成A常用到原料 ![]() ,现有相对分子质量最小的该原料的同系物X,检验X中碳碳双键的操作方法 , 写出X与银氨溶液发生的离子反应方程式 .
,现有相对分子质量最小的该原料的同系物X,检验X中碳碳双键的操作方法 , 写出X与银氨溶液发生的离子反应方程式 .
(3)B﹣C的反应类型为 .
(4)E﹣F的过程中常用HSCH2CH2CH2SH对E进行官能团保护,含﹣SH(巯基)叫硫醇,根据系统命名法,HSCH2CH2CH2SH的名称是
(5)同时满足以下条件的青蒿素的同分异构体共有种.
①常温下,能与NaHCO3溶液反应;②能与FeCl3溶液发生显色反应;③1mol该物质与足量的Na反应,产生2mol H2;④质谱与红外表明分子中含2个 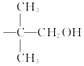 基团;
基团;
⑤苯环上只有一种化学环境的氢.
(6)参考上述合成路线,写出由苯甲醛和乙醇为原料,经三步制备3﹣苯基丙烯醛的合成路线(无机试剂任选). 合成路线示例是:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知MnO2和浓盐酸加热可以制取Cl2,某化学研究性学习小组拟用下列装置和药品制备无水氯化铁晶体,该物质极易潮解,100℃左右时升华。

请回答下列问题
(1)制备开始时A 装置烧瓶中产生的现象为_____;发生反应的离子 方程式为_____________________。
(2)按气流方向连接完整转置:a→___→___→___→___→b→c→___→___(填仪器接口字母编号)。____
(3)装置E的作用是_______;B装置硬质政璃管内导管口处棉花的作用是_________________。
(4)若无C装置可能产生的后果是________________________________。
(5)本实验合理的操作步骤为_____________________________(按操作顺序选择序号)
①添加药品②连接仪器③检查装置气密性④点燃A处酒精灯⑤点燃B处酒精灯⑥使B中硬质玻璃管内充满黄绿色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Y与Z为金属元素,四种元素的简单离子的电子层结构均相同.p、q是它们中的部分元素组成的化合物,r是W的单质,s是Z的单质.这些物质间的转化关系如图所示.下列说法不正确的是( ) 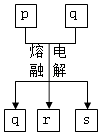
A.原子半径:Y>Z>W>X
B.q属于离子化合物
C.p能与盐酸反应,但不能与氢氧化钠溶液反应
D.一定条件下,r与s能发生化合反应生成p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列结构示意图,判断下列说法中不正确的是( ) 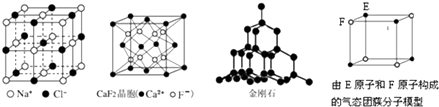
A.在NaCl晶体中,距Na+最近的多个Cl﹣构成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数之比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下:
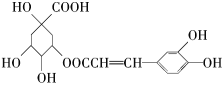
关于对咖啡鞣酸的下列叙述中,不正确的是( )
A.分子式为C16H18O9
B.与苯环直接相连的原子都在同一平面上
C.1mol咖啡鞣酸水解时可消耗8molNaOH
D.与浓溴水既能发生取代反应又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为一原电池装置,下列叙述中正确的是
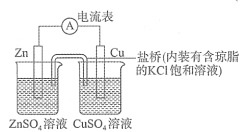
A.该装置中电子由Zn电极流向Cu电极,溶液中的![]() 通过盐桥移向Zn极
通过盐桥移向Zn极
B.将上述装置中的Zn棒和Cu棒同时浸入CuSO4溶液,电流表的指针偏转幅度变小,且很快减弱
C.将烧杯内溶液对换,电流表指针发生偏转
D.将盐桥改为铜导线连接两种溶液,电流由Cu电极移向Zn电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com