
【题目】氮及其化合物在生产、生活中有着重要的作用.请回答下列问题: 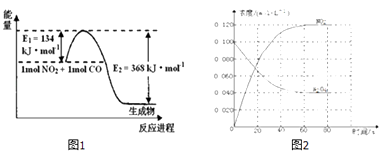
(1)图1是常温下1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(2)在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)2NO2(g)△H如图2
①在0﹣60s时段,反应速率v(N2O4)为molL﹣1s﹣1 .
②温度升高,混合气体的颜色变深,则△H0(填“>”或“<”).
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有(填字母).
a.向混合气体中通入N2O4 b.升高温度
c.向混合气体中通入NO2 d.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2 , 反应2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1的CH3COONa溶液.
①A、B两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为(已知HNO2的电离
常数Ka=7.1×10﹣4molL﹣1 , CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1).
②可使A、B两溶液的PH相等的方法是(填字母).
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(4)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平).0.6molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量为 .
【答案】
(1)NO2(g)+CO(g)=CO2(g)+NO(g)△H=﹣234kJ/mol
(2)0.001;>;ac
(3)c(NO3﹣)>c(NO2﹣)>c(CH3COO﹣);bc
(4)1.8mol
【解析】解:(1)该反应的焓变△H=E1﹣E2=134kJ/mol﹣368kJ/mol=﹣234kJ/mol,所以热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=﹣234kJ/mol,所以答案是:NO2(g)+CO(g)=CO2(g)+NO(g)△H=﹣234kJ/mol;(2)①由图可知,在0﹣60s时段△c(N2O4)=0.1mol/L﹣0.04mol/L=0.06mol/L,则v(N2O4)= ![]() =0.001mol/(L.min),
=0.001mol/(L.min),
所以答案是:0.001;
②温度升高,混合气体的颜色变深,说明升高温度平衡向生成NO2的方向移动,升高温度平衡向吸热反应移动,则△H>0,
所以答案是:>;
③a.向混合气体中通入N2O4 , 等效为在原平衡基础上增大压强到达的平衡,平衡逆向移动,N2O4的体积分数增大,故a正确;
b.正反应为吸热反应,升高温度平衡向正反应方向移动,N2O4的体积分数减小,故b错误;
c.向混合气体中通入NO2 , 等效为在原平衡基础上增大压强到达的平衡,N2O4的体积分数增大,故c正确;
d.使用高效催化剂缩短到达平衡的水解,不影响平衡移动,N2O4的体积分数不变,故d错误,
所以答案是:ac;(3)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,由2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液A中NaNO3物质的量浓度为0.1mol/L,NaNO2物质的量浓度为0.1mol/L,溶液B为0.1molL﹣1的CH3COONa溶液;
HNO2的电离常数Ka=7.1×10﹣4molL﹣1 , CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1 , 说明CH3COOH酸性小于HNO2的酸性,溶液中醋酸根离子水解程度大于亚硝酸根离子水解程度,溶液B碱性大于A溶液,两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为c(NO3﹣)>c(NO2﹣)>c(CH3COO﹣),
a.溶液B碱性大于A溶液,向溶液A中加适量水,稀释溶液,碱性减弱,不能调节溶液pH相等,故a错误;
b.向溶液A中加适量NaOH,增大碱性,可以调节溶液pH相等,故b正确;
c.向溶液B中加适量水,稀释溶液碱性减弱,可以调节溶液pH相等,故c正确;
d.溶液B碱性大于A溶液,向溶液B中加适量NaOH,溶液pH更大,故d错误;
所以答案是:c(NO3﹣)>c(NO2﹣)>c(CH3COO﹣);bc;(4)参加反应的硝酸转化为Cu(NO3)2、NO、NO2 , 根据Cu原子守恒可知n[Cu(NO3)2]=n(Cu)=0.6mol,得到的NO和NO2物质的量相同,根据电子转移守恒,则:3n(NO)+n(NO2)=0.6mol×2,故n(NO)=n(NO2)=0.3mol,根据氮原子守恒,可知n(HNO3)=2n[Cu(NO3)2]+n(NO)+n(NO2)=0.6mol×2+0.3mol+0.3mol=1.8mol,
所以答案是:1.8mol.
【考点精析】掌握化学平衡的计算是解答本题的根本,需要知道反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】下列是某学生自己总结的一些规律,其中正确的是( )
A. 氧化物不可能是还原产物,只可能是氧化产物
B. 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C. 饱和溶液一定比不饱和溶液的浓度大
D. 有些化学反应不属于化合、分解、置换、复分解等类型中的任何一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1(已知2KI+C12=2KCl+I2 , 碘与溴一样易溶于有机溶剂): 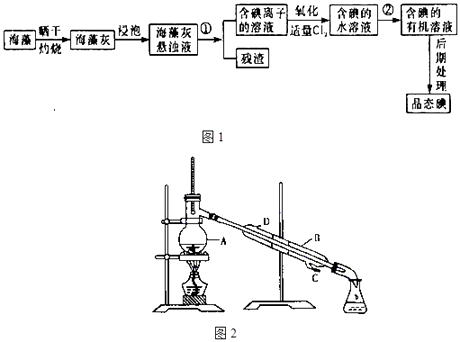
(1)图2中A 仪器的名称是 , 仪器B中冷凝水的水流方向: .
(2)提取碘的过程中,可供选择的有机试剂是 (填字母)
A.苯
B.四氯化碳
C.酒精
D.醋酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是()
A. NH4+、NO3-、A13+、Cl- B. Na+、Fe2+、K+、NO3-
C. MnO4-、K+、SO42-、Na+ D. K+、SO42-、HCO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,有的是药物,有的是香料.它们的结构简式如下所示: 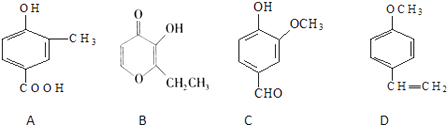
(1)化合物A的分子式是;A中含有的官能团的名称是;
(2)A、B、C、D四种化合物中互为同分异构体的是;
(3)化合物B的核磁共振氢谱中出现组峰;
(4)1molD最多能与mol的氢气发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H(布洛芬)是临床常用的镇痛消炎药,其合成路线如下(部分反应条件和试剂略):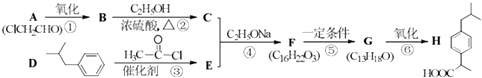
已知:(i) ![]() (R1、R2代表烷基)
(R1、R2代表烷基)
(ii) ![]() +ClCH2COOR4+R4ONa→
+ClCH2COOR4+R4ONa→ ![]() COOR4+R4OH+NaCl(R3、R4代表烷基)
COOR4+R4OH+NaCl(R3、R4代表烷基)
请回答下列问题:
(1)化合物H的分子式是 , 化合物B的官能团名称是 , 第③步的化学反应类型是 .
(2)第②步反应的化学方程式是 .
(3)化合物G的结构简式是 .
(4)第④步反应的化学方程式是 .
(5)同时满足下列条件的H的所有同分异构体的结构简式是 .
I.结构中有苯环,无﹣O﹣O﹣;II.核磁共振氢谱为4组峰,峰面积之比为2:2:1:1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1molL﹣1的盐酸滴定25.00mLNa2CO3溶液,其滴定曲线如图所示,下列说法正确的是( ) 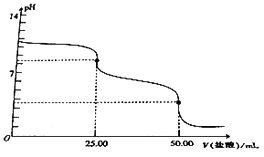
A.Na2CO3溶液的浓度为0.2molL﹣1
B.当V(盐酸)=0时,溶液中:c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3)
C.当V(盐酸)=25.00mL时,溶液中:c(Cl﹣)>c(HCO3﹣)>c(CO32﹣)>c(H2CO3)
D.当V(盐酸)=50.00mL时,溶液中:c(Na+)+c(H+)=c(OH﹣)+c(Cl﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com