
下列叙述正确的是
A.Li在氧气中燃烧主要生成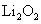
B.将SO2通入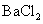 溶液可生成
溶液可生成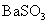 沉淀
沉淀
C.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu

【解析】A错误,因为Li在空气中燃烧只能生成Li2O,直接取材于第一册课本第二章第三节; B错误,酸性:HCl>H2SO3>H2CO3所以通入后无BaSO3沉淀,因为BaSO3+2HCl=BaCl2+H2O+SO2↑;D错误,溶液中该反应难以发生,先是:2NH3+2H2O+CuSO4=Cu(OH)2↓+(NH4)2SO4,接着Cu(OH)2 CuO+H20,溶液中NH3不能还原CuO为Cu,要还原必须是干燥的固态!C正确,强酸制弱酸,酸性:H2CO3>HClO,反应为:CO2+H20+Ca(ClO)2=CaCO3↓+2HClO,直接取材于课本第一册第四章第一节;
CuO+H20,溶液中NH3不能还原CuO为Cu,要还原必须是干燥的固态!C正确,强酸制弱酸,酸性:H2CO3>HClO,反应为:CO2+H20+Ca(ClO)2=CaCO3↓+2HClO,直接取材于课本第一册第四章第一节;
【答案】C



科目:高中化学 来源: 题型:
钛(Ti )被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:
 |
(l)电解饱和食盐水时,总反应的离子方程式是 。
(2)根据上面流程写出钛铁矿经氯化法得到四氯化钛的化学方程式
。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s) △H =-641kJ·mol-1
②Ti(s) + 2Cl2(g)=TiCl4(s) △H = -770kJ·mol-1
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s) △H= 。
反应2Mg(s) + TiCl4(s) 2MgCl2(s) + Ti,在Ar气氛中进行的理由是: 。
2MgCl2(s) + Ti,在Ar气氛中进行的理由是: 。
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊。则珍珠
中含有( )
A. 氯离子 B.硫酸根离子 C.碳酸根离子 D. 氢氧根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
| 选项 化合物 | A | B | C | D |
| Y | CO2 | Fe2O3 | C2H5OH | FeCl3 |
| W | MgO | Al2O3 | C2H5ONa | CuCl2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用钢材镀铝。工艺流程如下:

(注 :NaCl熔点为801℃;AlCl3在181℃升华)
:NaCl熔点为801℃;AlCl3在181℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为① 和② 。
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有 ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在 。
(3)在用废碱液处理A的过程中,所发生反应的离子方程式为 。
(4)镀铝电解池中,金属铝为 极,熔融盐电镀中铝元素和氯元素主要以AlCl4― 和Al2Cl7―形式存在,铝电镀的主要电极反应式为 。
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
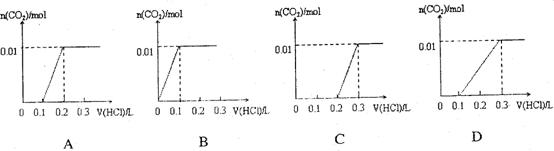

查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 。
(2)另称取铁钉6.0g放入15.0ml.浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除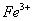 外还可能含有
外还可能含有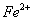 。若要确认其中的
。若要确认其中的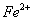 ,应先用 选填序号)。
,应先用 选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性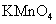 溶液
溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:
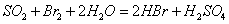
然后加入足量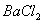 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中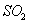 的体积分数为 。
的体积分数为 。
[探究二]
分析上述实验中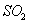 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有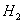 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
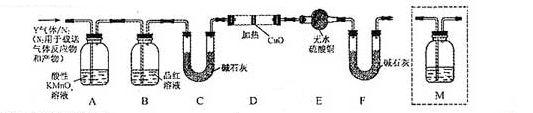
(3)装置B中试剂的作用是 。
(4)认为 气体Y中还含有Q的理由是 (用化学方程式表示)。
气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确 认Q的存在,需在装置中添加M于 (选填序号)。
认Q的存在,需在装置中添加M于 (选填序号)。
a. A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有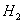 ,预计实验现象应是 。
,预计实验现象应是 。
(7)若要测定限定体积气体Y中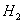 的含量(标准状况下约有28ml
的含量(标准状况下约有28ml 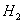 ),除可用测量
),除可用测量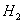 体积的方法外,可否选用质量称量的方法?做出判断并说明理由 。
体积的方法外,可否选用质量称量的方法?做出判断并说明理由 。

查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.Cl2通入NaOH溶液:
Cl2+OH-===Cl-+ClO-+H2O
B.NaHCO3溶液中加入稀盐酸:
CO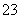 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:
Al3++4NH3·H2O===AlO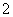 +4NH
+4NH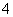 +2H2O
+2H2O
D.Cu溶于稀HNO3:
3Cu+8H++2NO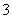 ===3Cu2++2NO↑+4H2O
===3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
合金是建造航空母舰的主体材料。
(1) 航母升降机可由铝合金制造。
① 铝元素在周期表中的位置为 。工业炼铝的原料由铝土矿提取而得。提取过程中通入的气体为 。
② Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为 。
焊接过程中使用的保护气为 (填化学式)。
(2) 航母舰体为合金钢。
① 舰体在海水中发生的电化学腐蚀主要为 。
② 航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为 。
(3) 航母螺旋桨主要用铜合金制造。
① 80.0gCu-Al合金用酸完全溶解后,加入过量氨水,过滤得白色沉淀39.0g,则合金中Cu的质量分数为 。
② 为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合题8图信息推断该合金中除铜外一定含有 。


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com