
【题目】海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如下:
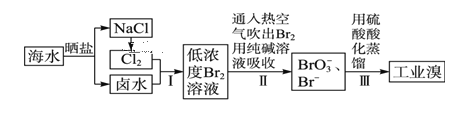
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_______。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的__________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:_____Br2+_____CO32-=_____ BrO3-+_____Br-+_____CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是__________。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
【答案】富集(或浓缩)溴元素 C 3 3 1 5 3 SO2+Br2+2H2O=2HBr+H2SO4 BD
【解析】
海水通过晒盐得到氯化钠和卤水,电解饱和氯化钠溶液得到氯气,卤水加入氧化剂氯气氧化溴离子得到低浓度的单质溴溶液,通入热空气或水蒸气吹出Br2,利用的是溴单质的易挥发性,用纯碱溶液吸收溴单质得到含Br-、BrO3-的溶液,再利用溴酸根离子和溴离子在酸性溶液中发生氧化还原反应得到溴单质,据此分析解答。
(1)步骤Ⅰ中已获得游离态的溴浓度很低,如果直接蒸馏,生产成本较高,不利于工业生产,步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是富集溴元素,降低成本,故答案为:富集溴元素;
(2)溴易挥发,步骤Ⅱ通入热空气或水蒸气吹出Br2,就是利用溴的挥发性,故答案为:C;
(3)该反应中Br元素化合价由0价变为-1价、+5价,其最小公倍数是5,再结合原子守恒或电荷守恒得方程式为:3Br2+3CO32-═BrO3-+5Br-+3CO2↑,故答案为:3;3;1;5;3;
(4)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的化学方程式为:Br2+SO2+2H2O=2HBr+H2SO4,故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶。A.乙醇易溶于水,所以不能作萃取剂,故A错误;B.四氯化碳符合萃取剂选取标准,所以能作萃取剂,故B正确;C.溴单质与烧碱溶液反应,不能做萃取剂,故C错误;D.苯符合萃取剂选取标准,所以能作萃取剂,故D正确;故选BD。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】Cu2SO3·CuSO3·2H2O是一种深红色固体(以下用M表示)。某学习小组拟测定胆矾样品的纯度,并以其为原料制备M。
已知:①M不溶于水和乙醇,100℃时发生分解反应;
②M可由胆矾和SO2为原料制备,反应原理为3Cu2++6H2O+3SO2![]() Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
I.测定胆矾样品的纯度。
(1)取w g胆矾样品溶于蒸馏水配制成250mL溶液,从中取25.00mL于锥形瓶中,加入指示剂,用c mol·L-1EDTA(简写成Na4Y)标准溶液滴定至终点(滴定原理:Cu2++Y4-====CuY2-),测得消耗了V mL EDTA标准溶液。则该胆矾样品的纯度为____________%(用含c、V、w的代数式表示)。如果滴定管装液前没有用EDTA标准溶液润洗,测得的结果会_________ (填“偏高”“偏低”或“无影响”)。
Ⅱ.制备M。实验装置如下图所示:

(2)实验室用70%硫酸与亚硫酸钠粉末在常温下制备SO2。上图A处的气体发生装置可从下图装置中选择,最合适的是________(填字母)。

(3)装置D中的试剂是____________。装置B中水浴加热的优点是____________________。
(4)实验完毕冷却至室温后,从锥形瓶中分离产品的操作包括:__________、水洗、乙醇洗、常温干燥,得产品Cu2SO3·CuSO3·2H2O。检验产品已水洗完全的操作是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于锌、铜和稀硫酸组成的原电池(如下图),下列说法错误的是
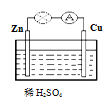
A. 负极电极反应式为Zn-2e- =Zn2+
B. 溶液中SO42-离子向负极移动
C. 电子由Zn片通过稀硫酸流向Cu片
D. 铜片上有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据A~E几种烃分子的结构填空。
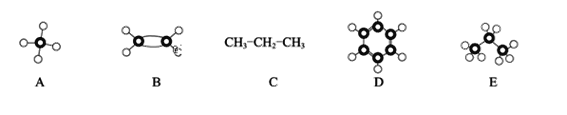
上述分子中属于C的同系物的是_____________(填字母序号)。
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是__________________(填字母序号,下同);
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于________________________;
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是__________。
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:
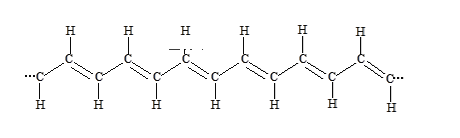
则合成该塑料的单体为___________ (填字母序号,下同);
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是__________;
A 加热分解法 B 电解法 C 高温还原法
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
实验序号 | A | B | C |
实验 内容 |
|
|
|
一周后,试管中铁钉锈蚀程度最大的是__________;
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过______mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或叙述正确的是
A. 1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642 kJ的热量:N2H4(l)+O2(g) ===N2(g)+2H2O(g) ΔH=+642 kJ·mol-1
B. 12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g) ===2CO(g) ΔH=-110.5 kJ·mol-1
C. 已知:H2(g)+ ![]() O2(g) ===H2O(l) ΔH=-286 kJ·mol-1,则:2H2O(l) ===2H2(g)+O2(g)的ΔH=+572 kJ·mol-1
O2(g) ===H2O(l) ΔH=-286 kJ·mol-1,则:2H2O(l) ===2H2(g)+O2(g)的ΔH=+572 kJ·mol-1
D. 已知N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量
2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应 3A(g)+2B(g)![]() zC(g)+2D(g)。在2L的密闭容器中把4molA和2molB混合,2min后反应达到平衡时生成1.6 mol C,又测得D的反应速率v(D)= 0.2 mol.L-1min-1。则下列说法不正确的是( )
zC(g)+2D(g)。在2L的密闭容器中把4molA和2molB混合,2min后反应达到平衡时生成1.6 mol C,又测得D的反应速率v(D)= 0.2 mol.L-1min-1。则下列说法不正确的是( )
A. z=4B. B的转化率是40%
C. A的平衡浓度是1.4mol.L-1D. 平衡时气体压强是原来的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标准状况),实验记录如表(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段反应速率最大_______min(填0~1、1~2、2~3、3~4、4~5)。反应开始后反应速率先增大的原因是__________。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率_______(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为不可行的是(_______)
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图

①该反应的化学方程式是____________。
②该反应达到平衡状态的标志是_________。
A.X、Y、Z的反应速率相等 B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变 D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“银-Ferrozine”法检测室内甲醛含量的原理如下:

下列说法错误的是( )
A. 标准状况下,11.2LCO2中含碳氧双键的数目为6.02×1023
B. 30gHCHO被氧化时转移电子数目为4×6.02×1023
C. 反应①的化学方程式为2Ag2O+HCHO=4Ag+CO2+H2O
D. 理论上,吸收HCHO 与消耗Fe3+的物质的量之比为4∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com