
【题目】【化学——选修5:有机化学基础】
高分子化合物H的合成路线如下图所示:

(1)A的名称是 ,由A生成B的反应类型是 。
(2)C的结构简式为 ,F中官能团的名称为 。
(3)写出由E生成M的化学方程式: 。
(4)在催化剂存在下,D、G按物质的量之比为1:1发生加聚反应的化学方程式为 。
(5)Q是M的一种同系物,相对分子质量比M大14,Q有多种同分异构体,则符合下列条件的同分异构体共有 种。
①能与金属钠发生置换反应;②能发生银镜反应。写出其中核磁共振氢谱有4组峰的一种同分异构体的结构简式 。
【答案】(1)1,2二溴乙烷 取代反应(或水解反应)
(2)![]() 羟基、溴原子
羟基、溴原子
(3)BrCH2CH=CHCH2Br + 2NaOH![]() HOCH2CH=CHCH2OH +2NaBr
HOCH2CH=CHCH2OH +2NaBr
(4)![]()
(5)12  ( 或
( 或 )
)
【解析】
试题分析:(1)C2H4为乙烯,由反应条件可得C2H4与溴水发生加成反应产生的A为1,2二溴乙烷,A与NaOH溶液加热发生水解反应生成B是乙二醇,结构简式是CH2OHCH2OH,该反应类型为取代或水解反应;
(2)B为乙二醇,由B与C反应的生成物结构简式可得C是苯甲醇,C的结构简式为![]() ;根据M的结构简式HOCH2CH=CHCH2OH及生成的HOOCCHBrCH2COOH,可知M与HBr发生加成反应,产生的F的结构简式为HOCH2CHBrCH2CH2OH,其中含有的官能团为羟基、溴原子;
;根据M的结构简式HOCH2CH=CHCH2OH及生成的HOOCCHBrCH2COOH,可知M与HBr发生加成反应,产生的F的结构简式为HOCH2CHBrCH2CH2OH,其中含有的官能团为羟基、溴原子;
(3)E为1,3丁二烯,该物质与溴的水溶液发生1,4加成,产生E,结构式为BrCH2CH=CHCH2Br,由E生成M的反应为E与NaOH溶液的水解反应,可得反应方程式是BrCH2CH=CHCH2Br + 2NaOH![]() HOCH2CH=CHCH2OH +2NaBr;
HOCH2CH=CHCH2OH +2NaBr;
(4)D的结构简式为![]() ,G的结构简式为HOOCCH=CHCOOH,二者按1:1发生加聚反应的方程式是
,G的结构简式为HOOCCH=CHCOOH,二者按1:1发生加聚反应的方程式是![]() ;
;
(5)M分子式是C4H8O2,化合物Q是M的同系物,比M相对分子质量大14,则Q的分子式是C5H10O2,能与钠反应,说明该物质含有羟基或羧基,能发生银镜反应,说明该物质含有醛基或甲酸酯基,根据氧原子数和不饱和度判断,应为一个醛基和一个羟基。碳骨架为: C—C—C—C—CHO、![]() 、
、![]() 、
、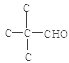 ,羟基在碳链上的连接方式分别有4种、4种、3种、1种,故共有12种同分异构体,其中羟基与
,羟基在碳链上的连接方式分别有4种、4种、3种、1种,故共有12种同分异构体,其中羟基与![]() 、
、 碳骨架结合形成的化合物
碳骨架结合形成的化合物 、
、 核磁共振氢谱中有4组峰。
核磁共振氢谱中有4组峰。


科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
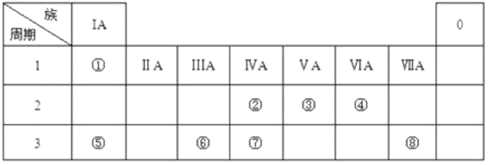
(1)地壳中含量最高的金属元素在周期表中的位置是 ;
(2)⑧形成的单质与水反应的离子方程式为 ;
(3)②⑦的非金属性强弱可通过比较这两种元素 (填编号)
a、原子的得电子能力
b、含氧酸的酸性
c、气态氢化物的稳定性
d、单质的熔点
(4)写出一种由④⑤⑧元素组成的既含离子键又含有共价键的物质的电子式 。
(5)化工行业最近合成了由②和③形成的化合物,其硬度比金刚石还大,该物质所形成的晶体还可能具有的性质或特点有 。(填编号)
①熔点很高 ②可以导电 ③不存在单个分子 ④具有空间网状结构
(6)①和③形成的某液态化合物摩尔质量与氧气相同,在常温常压下0.25mol该液态物质在足量的氧气中完全燃烧生成③的气态单质和液态水,同时放出QkJ的热量。写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1﹣氯丙烷跟NaOH的醇溶液共热,生成的产物再跟溴水反应,得到一种有机物,它的同分异构体有(除它之外)( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
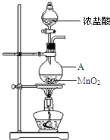
(1)仪器A的名称为_________;A中反应的离子方程式为______________________;
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | ____________________________ |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为______________________;
②不能证明产生的气体中含有HCl的实验是______________(填字母序号);
(3)已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因______________;
(4)已知:2S2O32-+I2═S4O62-+2I-.丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2.取25.00mL溶液X,加入过量KI溶液,然后用0.04molL-1 Na2S2O3溶液滴定生成
的I2,达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10molL-1 AgNO3溶液滴定所得溶液中的Cl-.
①X中的HClO不会影响I的测定结果,原因是_________________________;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10molL-1 AgNO3溶液的体积应大于____________________mL(用含V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、请根据如下图所示转化关系回答有关问题。A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有强氧化性。
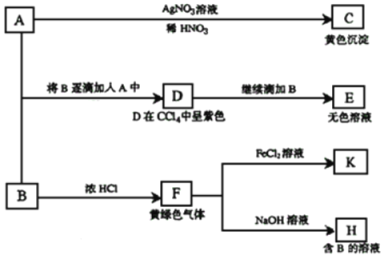
(1)写出A、B的化学式:A ,B 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
II、(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。在如下图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图像。

(2)将18.4gNaOH和NaHCO3固体混合物,在密闭容器中加热到约250℃,经充分反应后排出气体,冷却,称得剩余固体质量为16.6g。试计算混合物中NaOH的质量分数。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的应用极为广泛。利用如下图所示原电池可测量空气中Cl2的含量,其中电解质是Ag+可以自由移动的固体物质,下列分析正确的是
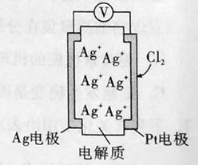
A.电流经外电路从Ag流向Pt电极
B.电池工作时,电解质中Ag+数目增多
C.正极反应:Cl2+2e-=2Cl-
D.空气中c(Cl2)越大,Ag极消耗速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比是化学学习与研究的常用方法。已知:NaH是一种离子化合物,与水反应放出氢气。下列关于铯(Cs)及其化合物的叙述不正确的是( )
A.无水醋酸铯的化学式为CH3COOCs,易溶于水,其水溶液显碱性
B.碳酸氢铯加热即分解生成碳酸铯、二氧化碳和水
C.在Na、K、Rb、Cs中,Cs熔点最高,密度最大
D.CsH是离子化合物,与水反应可以生成H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com