
【题目】完成原电池问题。
Ⅰ.有甲、乙两位同学均想利用原电池反应检测金属的活动性,两人均使用相同镁片与铝片作电极,甲同学将电极放入2 mol/L H2SO4 溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如图所示。

请回答:
(1)写出甲池中正极的电极反应式: 。
(2)写出乙池中负极的电极反应式和总反应的离子方程式:
负极: ;
总反应: 。
(3)如果甲、乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出______ 活动性更强,而乙会判断出______ 活动性更强(填写元素符号)。
(4)由此实验,可得到如下哪些正确结论?_________(填写字母序号)。
a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.上述实验反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”的做法是“不可靠”的
Ⅱ.市场上出售的“热敷袋”其主要成分是铁屑、炭粉、木屑和少量氯化钠、水等。“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。“热敷袋”放出的热量是利用了 而放出热量。
【答案】Ⅰ.(1)2H++2e-=H2↑
(2)Al+4OH--3e-=AlO2-+2H2O;2Al+2OH-+2H2O=2AlO2-+3H2↑
(3)Mg;Al
(4)ad
Ⅱ.铁屑、炭粉、空气(氧气)、NaCl溶液构成原电池,铁被氧化(合理即可)
【解析】
试题分析:Ⅰ.(1)甲中镁易失电子作负极、Al作正极,负极上镁发生氧化反应、正极上氢离子发生还原反应,负极反应为Mg-2e-=Mg2+,正极反应为2H++2e-=H2↑。
故答案为:2H++2e-=H2↑;
(2)乙池中铝易失电子作负极,负极上铝失电子发生氧化反应,电极反应式为:Al+4OH--3e-=AlO2-+2H2O,镁作正极,正极发生还原反应,总反应为2Al+2OH-+2H2O=AlO2-+3H2↑。
故答案为:Al+4OH--3e-=AlO2-+2H2O;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)甲中镁作负极、乙中铝作负极,根据作负极的金属活泼性强判断,甲中镁活动性强、乙中铝活动性强。
故答案为:Mg;Al;
(4)a.根据甲、乙中电极反应式知,原电池正负极与电解质溶液有关,故A正确;b.镁的金属性大于铝,但失电子难易程度与电解质溶液有关,故B错误;c.该实验说明电解质溶液性质影响电极的正负极,不能说明金属活动性顺序没有使用价值,故C错误;d.该实验说明化学研究对象复杂,反应与条件有关,电极材料相同其反应条件不同导致其产物不同,所以应具体问题具体分析,故D正确。
故答案为:ad。
Ⅱ.该装置符合原电池构成条件,所以能构成原电池。炭粉构成原电池正极,正极上氧气得电子发生还原反应,NaCl溶液起电解质溶液作用,从而形成原电池,加速Fe的氧化。放电时将化学能转化为电能,所以热敷袋放出的热来自于原电池中的氧化还原反应。
故答案为:铁屑、炭粉、空气(氧气)、NaCl溶液构成原电池,铁被氧化(合理即可)。


科目:高中化学 来源: 题型:
【题目】CO和联氨(N2H4)的性质及应用的研究是能源开发、环境保护的重要课题。
(1)①用CO、O2和KOH溶液可以制成碱性燃料电池,则该电池反应的离子方程式为________________。
②用CO、O2和固体电解质还可以制成如下图1所示的燃料电池,则电极d的电极反应式为______________。
(2)联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图2所示。
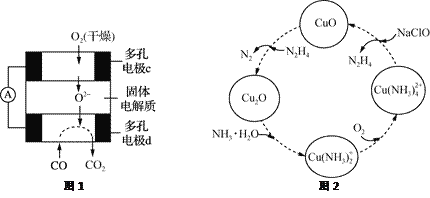
①在图示2的转化中,化合价不变的元素是_________(填元素名称)。
②在转化过程中通入氧气发生反应后,溶液的pH将________(填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为________。
③加入NaClO时发生的反应为:Cu(NH3)![]() +2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
+2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
该反应需在80℃以上进行,其目的除了加快反应速率外,还有________、________
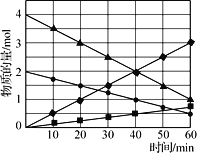
图3
(3)CO与SO2在铝矾土作催化剂、773 K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图3所示,写出该反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是(用NA代表阿伏加德罗常数的值)
A.任何条件下,16gCH4与18 g H2O所含有电子数均为10NA
B.19g的H3O+ 离子中含有的电子数为11NA
C.0.5mol/LH2SO4中的H+数为NA
D.22.4 L的CO气体与1 mol N2所含的电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方案错误的是( )
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO(g) | CO2(g) | NaOH溶液、浓H2SO4 | 洗气 |
B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
C | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
D | Na2CO3(s) | NaHCO3(s) | —— | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学查阅教材上的溶解性表时发现,CuCO3对应的为“—”,表示不存在或遇水就分解。已知铜离子的常见沉淀为Cu(OH)2(蓝色)、Cu2(OH)2SO4(蓝色)、Cu2(OH)2CO3(绿色)等,它们均不含结晶水。为了探究CuSO4和Na2CO3反应产物的成份,该同学按以下实验方法制备了两种沉淀,并设计了探究沉淀成份的实验。
取2个小烧杯和2个锥形瓶,在每个烧杯里加入50mL0.5mol/L的CuSO4溶液,在锥形瓶里分别加入40mL 和50mL0.5mol/LNa2CO3溶液,置于70℃水中水浴加热,然后将CuSO4溶液加入到Na2CO3溶液中,继续水浴,均有气泡产生,几分钟后分别得到蓝绿色和绿色沉淀。过滤、洗涤、干燥,得到两份固体。
I.对蓝绿色沉淀成份的探究。
通过右边实验证实,沉淀中含有Cu2(OH)2CO3和Cu2(OH)2SO4

(1)证明有Cu2(OH)2CO3存在的现象为____________;
(2)试剂①为__________,证明有Cu2(OH)2SO4存在的现象为______________。
II.对绿色沉淀成份的探究
重复I实验,发现没有SO42-存在,有Cu2(OH)2CO3存在;
通过下列实验证实,沉淀中只有Cu2(OH)2CO3

(3)该同学想通过测量固体分解所得气体的质量来确定沉淀的成份,按上述思路组装好装置,加入相应的药品,并指出所加药品的目的。

(4)按照该同学的设计思路,只需测定某两个装置的质量变化,即△m (_______):△m(_______)=_______时(括号中填写装置的序号)就可确定固体是Cu2(OH)2CO3。
(5)结论:n(Cu2+):n(CO32-)>1时,所得固体产物有Cu2(OH)2CO3和Cu2(OH)2SO4 ;n(Cu2+):n(CO32-)≤1时,所得固体产物全部是Cu2(OH)2CO3,生成该沉淀发生反应的离子方程式为:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】龙胆酸烷基酯类F是一种药物皮肤美白剂,合成路线如下:

(1)D(龙胆酸)中含氧官能团的名称为 、 。
(2)E →F的反应类型是 。
(3)写出D →E反应的化学方程式: 。
(4)写出满足下列条件的龙胆酸乙酯( )的一种同分异构体结构简式: 。
)的一种同分异构体结构简式: 。
Ⅰ.能发生银镜反应,与FeCl3不发生显色反应但其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.核磁共振氢谱有四组峰,且峰的面积之比为6:2:1:1。
(5)已知: 。水杨酸乙酯(
。水杨酸乙酯( )广泛应用于日用香皂等。根据已有知识并结合相关信息,写出以苯、乙醇为原料制备水杨酸乙酯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)广泛应用于日用香皂等。根据已有知识并结合相关信息,写出以苯、乙醇为原料制备水杨酸乙酯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有下列六种离子:①HCO3- ②SO32- ③Na+ ④CO32- ⑤NH4+ ⑥NO3-,向其中加入一定量Na2O2后,溶液中离子浓度基本保持不变的是( )
A.只有⑥ B.④⑥ C.③④⑥ D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是

A. 双酚A的分子式是C15H16O2
B. 双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3
C. 反应①中,1 mol双酚A最多消耗2 mol Br2
D. 反应②的产物中只有一种官能团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com