
升高温度时,化学反应速率加快,主要原因是
A.分子运动速率加快,使该反应物分子的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.该化学反应的过程是吸热的
D.该化学反应的过程是放热的
科目:高中化学 来源:2014-2015学年广东省广州市高一上学期期中化学试卷(解析版) 题型:选择题
下列物质中,含有自由移动Cl-的是
A.KClO3溶液 B.液态HCl C.熔融NaCl D.KCl晶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
下列关于 0.2 mol/L 硝酸钾溶液的叙述中,正确的是( )
A.1 L 该溶液中含硝酸钾 202 g
B.100 mL 该溶液中含硝酸钾 0.02 mol
C.从 1 L 该溶液中取出 500 mL 后,剩余溶液的浓度为 0.1 mol/L
D.1 L 水中溶解 0.2 mol 硝酸钾,即可配得 0.2 mol/L 硝酸钾溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
在一密闭容器中,等物质的量的A和B发生反应:A(g)+2B(g) 2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
A.40% B.50% C.60% D.70%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的反应热ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+566.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:填空题
第三周期元素A、B、C,其原子序数依次增大,已知A的焰色为黄色,C的某种氧化物是形成酸雨的主要原因,且这三种元素的最高价氧化物的水化物有一种具有两性,且他们两两之间都能反应生成盐和水。
(1)填出元素符号A __________B __________C__________
(2) C 2- 离子结构示意图为
(3)A和C形成的化合物的电子式为 ,属于 化合物。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.苯的分子是环状结构,其性质跟环烷烃相似
B.苯分子的结构中含有碳碳双键,因此苯的性质跟烯烃相同
C.苯的分子式为C6H6,分子中的氢原子远远没有饱和,因此能和溴水反应
D.苯不能使酸性KMnO4溶液褪色,而大多数苯的同系物却可以使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高二上学期联考化学试卷(解析版) 题型:填空题
(16分)盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。
已知室温下:Ka(CH3COOH)=1.7×10-5 mol·L-1 ;H2CO3的电离常数Ka1=4.2×10-7mol·L-1 、 Ka2=5.6×10-11mol·L-1
(1)①请用离子方程式解释碳酸氢钠水溶液显碱性的原因 。
②常温下,物质的量浓度相同的下列四种溶液:
a、碳酸钠溶液 b、醋酸钠溶液 c、氢氧化钠溶液 d、氢氧化钡溶液。
其PH由大到小的顺序是: (填序号)。
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是 ;该醋酸溶液稀释过程中,下列各量一定变小的是 。
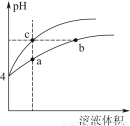
a.c(H+) b.c(OH-)
c.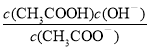 d.
d.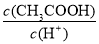
(3)以0.10 mol·L-1NaOH为标准液,测定某盐酸的浓度。取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | 氢氧化钠溶液的浓度 (mol·L-1) | 滴定完成时,氢氧化钠溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 24.12 | 20.00 |
2 | 0.10 | 23. 88 | 20.00 |
3 | 0.10 | 24.00 | 20.00 |
①滴定达到终点的标志是___________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为__________________。
(4)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw= mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市普高高二上学期期中理科化学试卷(解析版) 题型:填空题
化学计量在化学中占有重要地位,请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与 个H2O分子中所含原子数相等。
(2)含0.4 mol A13+的Al2(SO4)3中所含的SO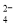 的物质的量是 _____ 。
的物质的量是 _____ 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为 ____________ 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是______________。
(5)某盐混合溶液中含有离子:Na+、Mg2+ 、Cl-、SO42-,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则 c(SO42-)=___________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com