
【题目】乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成.回答下列问题:
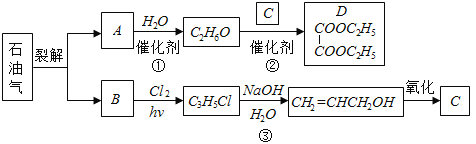
(1)B和A为同系物,B的结构简式为 .
(2)反应①的化学方程式为 ,其反应类型为 .
(3)反应③的反应类型为 .
(4)C的结构简式为 .
(5)反应②的化学方程式为 .
【答案】(1)B和A为同系物,B的结构简式为 CH2=CHCH3 .(2分)
(2)反应①的化学方程式为 CH2=CH2+H2O![]() CH3CH2OH ,(3分)其反应类型为 加成反应 .(1分)
CH3CH2OH ,(3分)其反应类型为 加成反应 .(1分)
(3)反应③的反应类型为 水解反应或取代反应 .(1分)
(4)C的结构简式为 HOOC﹣COOH .(2分)
(5)反应②的化学方程式为 HOOC﹣COOH+2CH3CH2OH![]() CH3CH2OOCCOOCH2CH3+2H2O .
CH3CH2OOCCOOCH2CH3+2H2O .
【解析】
试题分析:C2H6O与C反应生成D,由D可知C是HOOC-COOH,C2H6O是C2H5OH,则A是CH2=CH2,与水发生加成反应生成C2H5OH;C3H5Cl发生水解反应生成CH2=CH-CH2OH,C3H5Cl的结构为CH2=CH-CH2Cl;B为CH2=CH-CH3;CH2=CH-CHO氧化得HOOC-COOH;由以上分析可知(1)B的结构简式为CH2=CHCH3.
(2)反应①是乙烯与水生成乙醇,化学方程式为CH2=CH2+H2O![]() CH3CH2OH,其反应类型为加成反应.
CH3CH2OH,其反应类型为加成反应.
(3)反应③是CH2=CH-CH2Cl水解生成CH2=CH-CH2OH,反应类型为取代反应.
(4)C的结构简式为HOOC﹣COOH.
(5)反应②是乙二酸与乙醇生成乙二酸二乙酯,化学方程式为HOOC﹣COOH+2CH3CH2OH![]() CH3CH2OOCCOOCH2CH3+2H2O。
CH3CH2OOCCOOCH2CH3+2H2O。


科目:高中化学 来源: 题型:
【题目】某酸溶液的pH=3,则该酸溶液的物质的量浓度为( )
A.一定大于0.001 mol·L-1 B.一定等于0.001 mol·L-1
C.一定小于0.001 mol·L-1 D.以上说法均欠妥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在古代,我国人民就积累了不少对化学物质变化的认识。例如,晋代炼丹家、医学家葛洪所著《抱朴子》一书是中国为世界科技花园贡献出的一颗璀璨明珠,书中记载有“丹砂烧之成水银,积变又成丹砂”。 这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是
A.这个过程只涉及物理变化 B.这个过程是可逆反应
C.这个过程发生了复分解反应 D.“丹砂烧之成水银”过程中还可能产生SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示转化关系(X代表卤素),说法正确的是

A.H2(g)+ X2(g)===2H(g)+ 2X(g) △H2>0
B.生成HX的反应热与途径有关,所以△H1≠△H2 + △H3
C.若X分别表示Cl,Br,I,则过程Ⅱ吸收的热量依次增多
D.△H1代表H2的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol M气体和3 mol N气体混合发生下列反应2M(g)+ 3N(g)![]() xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是
xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是
A.x值为2
B.混合气体的密度增大
C.平衡时N的浓度为 0.6 mol/L
D.N的转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回归、改进、拓展教材实验,是高考化学实验考查的常见形式。
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。

II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):
![]()
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+ 对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol的镁、铝混合物溶于100 mL 2 moI/LH2SO4溶液中,然后再滴加l mol/LNaOH溶液。请回答:
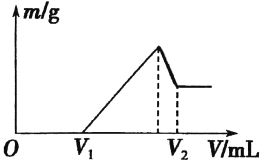
(l)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)=_________ mol,V2=________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL2mol/L1硫酸溶解此混合物后,再加入450 mL l moI/LNaOH溶液,所得沉淀中无A1(OH)3。满足条件的a的取值范围是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在20℃ 时,某气态烃与氧气混合装入密闭容器中,点燃爆炸后,又恢复到20℃ 。此时容器内气体的压强为反应前的一半,经NaOH溶液吸收后,容器内几乎真空。此烃的化学式可能是
A.CH4 B.C3H4 C.C2H4 D.C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.3gNa、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672ml混合气体,将该混合气体通过放电恰好反应,则原混合物中Na、Na2O、Na2O2的物质的量之比为( )
A: 1:2:1 B: 1:1:1 C: 1:3:1 D: 4:3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com