
 ,丙的电子式为
,丙的电子式为 ;E在周期表中的位置为第三周期VA族;
;E在周期表中的位置为第三周期VA族;分析 A、B、C、D、E、F为短周期元素,且原子序数依次增大,A是原子半径最小的元素,则A为H元素;B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲,则为B为N元素,甲为NH4NO3;E与B同主族,则E为P元素;C的阳离子与F的阴离子相差一个电子层,结合原子序数可知,C、D均处于第三周期,F原子序数大于P,且可形成阳离子、阴离子个数比为2:1的离子化合物丙,故F为S、C为Na、丙为Na2S;A与D可以按照原子个数比4:1形成化合物乙,且乙分子中含有18个电子,则D为Si、乙为SiH4,以此解答该题.
解答 解:A、B、C、D、E、F为短周期元素,且原子序数依次增大,A是原子半径最小的元素,则A为H元素;B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲,则为B为N元素,甲为NH4NO3;E与B同主族,则E为P元素;C的阳离子与F的阴离子相差一个电子层,结合原子序数可知,C、D均处于第三周期,F原子序数大于P,且可形成阳离子、阴离子个数比为2:1的离子化合物丙,故F为S、C为Na、丙为Na2S;A与D可以按照原子个数比4:1形成化合物乙,且乙分子中含有18个电子,则D为Si、乙为SiH4,
(1)D为Si,原子结构示意图为 ,丙为Na2S,电子式为
,丙为Na2S,电子式为 ,E为P元素,在周期表中的位置为:第三周期VA族,
,E为P元素,在周期表中的位置为:第三周期VA族,
故答案为: ;
; ;第三周期VA族;
;第三周期VA族;
(2))①乙为SiH4,分子只含有极性共价键,故正确;
②钠离子比气体非金属离子少一个电子层,离子半径最小,故错误;
③非金属性B(N)>E(P),故B的氢化物更稳定,故正确;
④甲为NH4NO3,含有离子键、共价键,丙为Na2S,只含有离子键,故错误,
故答案为:①③;
(3)SO2通入BaCl2和HNO3的混合溶液中,HNO3将SO2氧化为SO42-,NO3-本身被还原为NO,SO42-与Ba2+结合生成白色沉淀,反应的离子方程式为3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+,
故答案为:3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+;
(4)以上元素组成的10电子微粒有NH3、Na+、NH4+,18电子微粒有SiH4、PH3、H2S、HS-、S2-.能相互反应的有2NH3+H2S═2NH4++S2-或NH3+HS-═NH4++S2-或NH3+H2S═NH4++HS-,
故答案为:2NH3+H2S═2NH4++S2-或NH3+HS-═NH4++S2-或NH3+H2S═NH4++HS-.
点评 本题考查位置结构与性质关系的综合应用,题目难度中等,涉及常用化学用语、元素周期律、元素化合物性质、盐类水解等,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属铝溶于稀硫酸中:Al+2H+═A13++H2↑ | |
| B. | 少量Cl2通入KI溶液中:Cl2+2I-═2C1-+I2 | |
| C. | 醋酸钠水溶液中通入足量CO2:2CH3COO-+CO2+H2O═2CH3COOH+CO32- | |
| D. | 碳酸锌溶于稀硝酸中:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中:c2(H+)≠c(H+)•c(A-)+Kw | |
| B. | 由pH=3的HA溶液与pH=11的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA和NaA溶液等体积混合,所得溶液中:c(A-)>c(HA)>c(Na+)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液与0.05 mol•L-1 NaOH溶液等体积混合,所得溶液中:2c(H+)+c(HA)═c(A-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

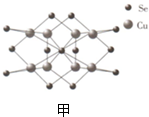

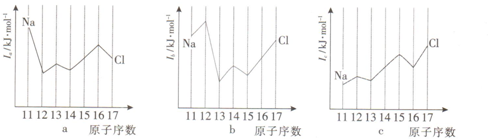
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
铬、铁、镍、铜等金属及其化合物在工业上有重要用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数为34 | |
| B. | 最高价氧化物的水化物的分子式为:H2SeO4 | |
| C. | Se的非金属性比Br强 | |
| D. | 气态氢化物的稳定性比硫化氢气体弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com