
【题目】有机物A由碳、氢、氧三种元素组成.现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g.回答下列问题:
(1)3gA中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式.
(3)写出有机物A可能的结构简式.
【答案】
(1)解:浓硫酸增重3.6g为水的质量,n(H2O)= ![]() =0.2mol,根据H原子守恒可知n(H)=2n(H2O)=0.4mol,
=0.2mol,根据H原子守恒可知n(H)=2n(H2O)=0.4mol,
碱石灰增重4.4g为二氧化碳的质量,n(CO2)= ![]() =0.1mol,
=0.1mol,
4.48L氧气的物质的量= ![]() =0.2mol,氧气的质量=0.2mol×32g/mol=6.4g
=0.2mol,氧气的质量=0.2mol×32g/mol=6.4g
故CO的质量=3g+6.4g﹣3.6g﹣4.4g=1.4g,故 n(CO)= ![]() =0.05mol,
=0.05mol,
根据C原子守恒可知n(C)=n(CO2)+n(CO)=0.1mol+0.05mol=0.15mol,
答:3gA中所含氢原子、碳原子的物质的量各是0.4mol、0.15mol
(2)解:由O原子守恒可知3gA中n(O)=2n(CO2)+n(CO)+n(H2O)﹣2n(O2)=2×0.1 mol+0.05 mol+0.2 mol﹣2×0.2 mol=0.05mol,
由(1)(2)可知3gA中3g A中,n(H)=0.4mol,n(C)=0.15mol,
所以,n(C):n(H):n(O)=3:8:1,故A的最简式为C3H8O,由H原子与碳原子数目可知,H原子已经饱和C原子四价结构,故其最简式即为分子式,A的分子式为C3H8O,
答:该有机物的分子式为C3H8O
(3)解:有机物的分子式为C3H8O,为醇或醚,可能结构简式为CH3CH2CH2OH、CH3CHOHCH3、CH3OCH2CH3,
答:有机物A可能的结构简式为CH3CH2CH2OH、CH3CHOHCH3、CH3OCH2CH3
【解析】(1)浓硫酸增重3.6g为水的质量,根据n= ![]() 计算水的物质的量,根据H原子守恒计算n(H);
计算水的物质的量,根据H原子守恒计算n(H);
碱石灰增重4.4g为二氧化碳的质量,根据n= ![]() 计算二氧化碳,根据n=
计算二氧化碳,根据n= ![]() 计算氧气的物质的量,根据m=nM计算氧气的质量,根据质量守恒计算CO的质量,根据n=
计算氧气的物质的量,根据m=nM计算氧气的质量,根据质量守恒计算CO的质量,根据n= ![]() 计算CO的物质的量,再根据C原子守恒计算n(C);(2)根据氧原子守恒3gA中氧原子的质量,再根据(1)(2)中的计算确定该物质的最简式及分子式;(3)有机物含C、H、O元素,为醇或醚.
计算CO的物质的量,再根据C原子守恒计算n(C);(2)根据氧原子守恒3gA中氧原子的质量,再根据(1)(2)中的计算确定该物质的最简式及分子式;(3)有机物含C、H、O元素,为醇或醚.


科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g) ![]() 2C(g)+D(s),所得实验数据如下表:
2C(g)+D(s),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(A) | n(B) | n(C) | ||
① | 600 | 0.30 | 0.20 | 0.30 |
② | 700 | 0.20 | 0.30 | 0.24 |
③ | 800 | 0.10 | 0.10 | a |
下列说法不正确的是
A. 实验①中,若5min时测得n(B)=0.050mol,则0至5min时间内平均反应速率v(A)=0.015mol/(L·min)
B. 实验②中达到平衡后,增大压强,A的转化率不变,平衡常数不变
C. 700℃时该反应的平衡常数K=4.0
D. 实验③中,达到平衡时,a>0.10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律表述正确的是
A. 原子序数为15的元素的最高化合价为+3
B. 第ⅦA族元素是同周期中非金属性最强的元素
C. Li、 Na、K、Rb、Cs的得电子能力逐渐增强
D. 原子序数为16的元素位于元素周期表的第三周期的IVA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是
A. 甲、乙中都是铝过量 B. 甲中铝过量,乙中碱过量
C. 甲中酸过量,乙中铝过量 D. 甲中酸过量,乙中碱过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL0.10mol·L-1Na2SO3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则SO32-将转化为
A.SO42-B.SC.SO2D.S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是中学化学中常见的单质,B、C为化合物,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列判断不正确的是
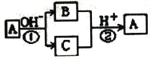
A. A、B、C一定含有一种相同的元素 B. A可能是金属,也可能是非金属
C. B、C的水溶液可能呈碱性或中性 D. 反应①和②一定都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁发生吸氧腐蚀时,正极发生的反应是( )
A.2H++2e﹣═H2↑
B.2H2O+O2+4e﹣═4OH﹣
C.Fe﹣3e═Fe3+
D.Fe﹣2e═Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨在材料领域有重要应用,某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用工艺如下:

(注:SiCl4的沸点是57.6C,金属氯化物的沸点均高于150C)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是______________________。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体I中生成的气体除氯化物外,还有______________________(填化学式)。气体II通入NaOH溶液中得到水玻璃的化学反应方程式为________;
(3)步骤①为:搅拌、_______________;
(4)由溶液IV生成沉淀V的总反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学对由NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等):
50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
m(混合物) | 9.2g | 15.7g | 27.6g |
标准状况下,V(CO2) | 2.24L | 3.36L | 3.36L |
(1)盐酸的物质的量浓度为_________。
(2)混合物中,n(NaHCO3):n(KHCO3)=_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com