
【题目】某工厂利用下列工艺以废旧铅蓄电池中含铅废料(主要含Pb、PbO、PbO2、PbSO4) 和稀H2SO4为原料制备高纯Pb、PbO等,实现铅的再生利用。其主要流程如下:
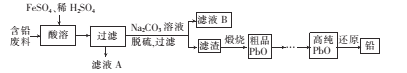
(1)含铅废料需要进行粉碎处理,其原因是____。
(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成PbSO4。若生成1 mol PbSO4,则转移电子的物质的量为__mol。
(3)向滤液B中加入Na2CO3溶液能形成悬浊液,此时溶液中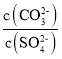 =____。若再向此悬浊液中加入少量Pb(NO3)2固体,则
=____。若再向此悬浊液中加入少量Pb(NO3)2固体,则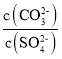 将会 ___(填“增大”“减小”或“不变”)[Ksp(PbSO4)=1.8×10-8;Ksp(PbCO3)=3.6×10-14]
将会 ___(填“增大”“减小”或“不变”)[Ksp(PbSO4)=1.8×10-8;Ksp(PbCO3)=3.6×10-14]
(4)铅易造成环境污染。水溶液中铅的存在形态与水溶液pH的关系如图a所示。pH由7变化到6时,不同形态铅之间转化的离子方程式为_________________
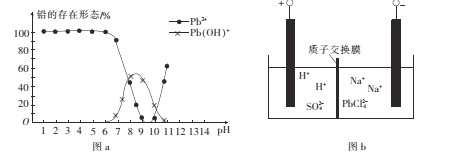
(5)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,进一步电解Na2PbC14溶液生成Pb,如图b所示。
①阴极的电极反应式为 ___。
②电解一段时间后,Na2PbC14的浓度明显下降,为了增大其浓度且实现物质的循环利用,可在阴极区采取的方法是____。
【答案】增大固体反应物的表面积或增大固体反应物的表面积,加快反应速率 1 2.0×10-6 不变 Pb(OH)++H+=Pb2++H2O PbCl42-+2e-=Pb+4Cl- 继续向阴极区增加PbO粗品
【解析】
含铅废料主要含Pb、PbO、PbO2、PbSO4,酸溶中加入FeSO4和稀硫酸,得到PbSO4,加入Na2CO3溶液,脱硫,则发生PbSO4+CO32-![]() PbCO3+SO42-,滤渣为PbCO3,然后煅烧得到PbO,通过热还原法得到Pb,据此分析;
PbCO3+SO42-,滤渣为PbCO3,然后煅烧得到PbO,通过热还原法得到Pb,据此分析;
(1)粉碎的目的是增大固体反应物的表面积或增大固体反应物的表面积,加快反应速率;
(2)酸溶,在Fe2+催化下,发生Pb+PbO2+2H2SO4=2PbSO4+2H2O,生成1molPbSO4时,消耗0.5molPb或PbO2,因此转移电子物质的量为0.5mol×2=1mol;
(3)根据(2)过滤中得到滤渣为PbSO4,加入Na2CO3溶液中发生PbSO4+CO32-![]() PbCO3+SO42-,滤液B中应含有Pb2+、CO32-、SO42-,向滤液B中加入Na2CO3溶液能形成悬浊液,此时溶液中
PbCO3+SO42-,滤液B中应含有Pb2+、CO32-、SO42-,向滤液B中加入Na2CO3溶液能形成悬浊液,此时溶液中![]() =2.0×10-6;向此悬浊液中加入少量Pb(NO3)2固体,温度保持不变,溶度积保持不变,该比值不变;
=2.0×10-6;向此悬浊液中加入少量Pb(NO3)2固体,温度保持不变,溶度积保持不变,该比值不变;
(4)根据图像,溶液显酸性时,Pb元素以Pb2+形式存在,pH由7变化到6时,Pb(OH)+转化为Pb2+,其转化离子方程式为Pb(OH)++H+=Pb2++H2O;
(5)①根据题意,PbCl42-溶液生成Pb,得到电子,发生还原反应,根据电解原理以及图b,阴极反应式为PbCl42-+2e-=Pb+4Cl-;
②根据图b,阳极反应式为2H2O-4e-=O2↑+4H+,H+从左向右移动,PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,在阴极采取的方法是继续向阴极区增加PbO粗品。


科目:高中化学 来源: 题型:
【题目】五氧化二钒(V2O5)在冶金、搪瓷、磁性材料等领域具有重要的应用。实验室以含钒废料(含有V2O3、CuO、MnO、SiO2、有机物)为原料制备V2O5的工艺流程如图所示。

已知:Ⅰ.含钒离子在溶液中的主要存在形式与溶液pH的关系如下表所示。
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要存在形式 | VO2+ | VO3- | V2O74- | VO43- |
Ⅱ.25℃时,部分难溶电解质的溶度积常数如下表所示。
难溶电解质 | Cu(OH)2 | Mn(OH)2 |
溶度积常数(Ksp) | 4.8×10-20 | 4×10-14 |
Ⅲ.25℃时,NH4VO3的溶解度为0.4gL-1;70℃时,NH4VO3的溶解度为63gL-1。
请回答下列问题:
(1)“焙烧”的目的是___。
(2)滤渣1的用途为___(任写一种)。
(3)“调pH”的目的除了使Cu2+沉淀完全外,还有___;调节pH为7时,Cu2+是否沉淀完全?___。(写出计算过程,当溶液中离子浓度小于10-5molL-1时,认为该离子沉淀完全)
(4)“沉锰”时,需将温度控制在70℃左右,温度不能过高或过低的原因为___。
(5)“浓缩结晶”后,需对所得NH4VO3进行洗涤、干燥。洗涤剂宜选用___;证明NH4VO3已洗涤干净的实验操作及现象为___。
(6)“煅烧”时,生成无污染性气体,该反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并注明(1)、(2)、(3)的反应类型
(1)由乙烯制备聚乙烯的反应 _______________反应类型:_________________
(2)用甲苯制TNT的反应 __________________反应类型:_________________
(3)溴乙烷与NaOH的乙醇溶液共热 _________________反应类型:_____________
(4)烯烃在一定条件下氧化时,由于C=C键断裂,转化为醛、酮,如:![]() 。若
。若![]() 在上述类似条件下发生反应,请写出反应的方程式 _________________________ 。
在上述类似条件下发生反应,请写出反应的方程式 _________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某石油化工产品X的转化关系如图,下列判断不正确的是( )
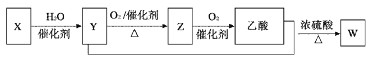
A. X可以发生加聚反应B. Y能与钠反应产生氢气
C. Z与CH3OCH3互为同分异构体D. W的结构简式为CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、X、D、E五种有机物的有关信息。
A | A的结构简式为 |
B | ①能使溴的四氯化碳溶液褪色 ②比例模型为 |
C | ①由C、H两种元素组成 ②球棍模型为 |
D | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 |
E | ①由C、H、O三种元素组成 ②球棍模型为 |
(1)B与溴的四氯化碳溶液反应的生成物的名称是___。
(2)写出在浓硫酸作用下,C与浓硝酸反应的化学方程式___。
(3)A与足量NaOH溶液共热发生皂化反应的化学方程式是___。
(4)若以B为主要原料合成乙酸,其合成路线如图所示:
![]()
①F物质官能团的名称是___。
②写出反应②的化学方程式___,反应类型为___。
③工业上以B为原料可以合成一种有机高分子,写出反应的化学方程式___。
(5)写出D与E反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是(NA表示阿伏加德罗常数)( )
A.常温c(OH-)/c(H+)=10-13的溶液中可能含有K+、Fe2+、NO3-、Cl-四种离子
B.1 L 0.1molL-1的CH3COONa溶液中CH3COO-和OH-的总数大于0.1NA
C.电子工业上用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3+ +Cu = Fe2++Cu2+
D.H2的燃烧热为a kJ·mol-1,H2燃烧热的热化学方程式为:O2(g) +2H2(g) = 2H2O(l) ΔH = -2a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知

A. X、Y、Z中最简单氢化物稳定性最弱的是Y
B. Z元素氧化物对应水化物的酸性一定强于Y
C. X元素形成的单核阴离子还原性大于Y
D. Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B. 乙烯与溴加成反应的产物为溴乙烷
C. 1 mol苯恰好与3 mol氢气完全加成,说明苯分子中有三个碳碳双键
D. 当n=7,主链上有5个碳原子的烷烃共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用电解原理,间接氧化降解处理含有机污染物的废水,其原理如图所示:
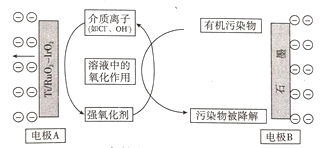
下列有关说法不正确的是( )
A.电极A是阳极,发生氧化反应
B.强氧化剂可能为Cl2、O2
C.有机污染物在石墨电极上被还原为无污染物
D.若介质离子为OH-,电极B上发生的反应为2H2O+2e- ═ H2↑+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com