
 Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上.
Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |
| 足量的钠 |
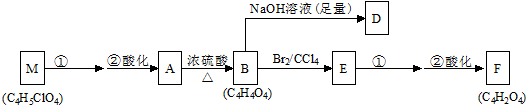
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳极为纯净气体,阴、阳两极产生的气体体积比≤1:1 |
| B、阳极为纯净气体,阴、阳两极产生的气体体积比≥1:1 |
| C、阳极为混合气体,阴、阳两极产生的气体体积比≤1:1 |
| D、阳极为混合气体,阴、阳两极产生的气体体积比≥1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用肉眼观察区别溶液、胶体和浊液 |
| B、用BaCl2溶液鉴别Na2SO3是否变质 |
| C、用澄清石灰水鉴别Na2CO2溶液和NaHCO3溶液 |
| D、用NaOH除去Mg中混有的少量Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/mol?L-1 | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/mol?L-1 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| v/mol?L-1?s-1 | 0.00760 | 0.0153 | 0.0227 | 0.0151 | 0.0228 |
| A、0.0380 mol?L-1?s-1 |
| B、0.152 mol?L-1?s-1 |
| C、0.608 mol?L-1?s-1 |
| D、0.760 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
序号 | 待测溶液体积(单位:mL) | 所消耗盐酸体积(单位:mL) | ||
| 滴定前 读数 | 滴定后 读数 | 消耗盐酸体积 | ||
| 1 | 20.00 | 0.50 | 20.60 | V(平)= |
| 2 | 20.00 | 6.00 | 26.00 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
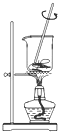 | 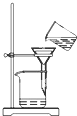 | 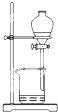 | 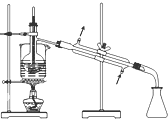 |
| A.将海带灼烧成灰 | B.过滤得含I-溶液 | C.萃取后放出碘的CCl4溶液 | D.分离碘并回收CCl4 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、K=
| ||
B、K=
| ||
C、K=
| ||
D、K=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com