
【题目】在NH3、HNO3、H2SO4的工业生产中,具有的共同点是 ( )
A.使用吸收塔设备B.使用尾气吸收装置
C.使用H2作原料D.使用催化剂
科目:高中化学 来源: 题型:
【题目】KClO3和KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快。如图为反应速率v(ClO3-)随时间(t)的变化曲线。下列有关说法不正确的是( )

A. KClO3和KHSO3发生反应的氧化剂与还原剂的物质的量之比为1∶3
B. 反应开始阶段速率逐渐增大可能是c(H+)逐渐增高导致的
C. 反应后期速率逐渐减小的主要原因是c(ClO3-)、c(HSO3-))降低
D. 纵坐标为v(HSO3-)时的v-t曲线与原图曲线完全吻合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年中国汽车销量大幅增长,同时也带来了严重的空气污染.汽车尾气装置中,气体在催化剂表面吸附与解吸的过程如图所示,下列说法正确的是( ) 
A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.NO和O2必须在催化剂表面才能反应
D.催化转化总反应为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列陈述I、Ⅱ均正确且具有因果关系的是
选项 | 陈述I | 陈述Ⅱ |
A. | SO2具有漂白性 | SO2可使溴水褪色 |
B. | NH3具有碱性 | NH3极易溶于水 |
C. | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
D. | HNO3具有酸性 | 可用铁和稀HNO3制取氢气 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在杠杆的两端分别挂着质量、体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图所示,则下列说法正确的是( ) 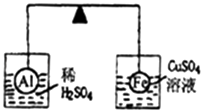
A.铝球一定是空心的
B.左边烧杯中的溶液质量减少了
C.去掉两烧杯杠杆仍平衡
D.右边铁球上出现红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烯烃和HBr发生加成反应能得到1种产物的是( )
A. CH2=C(CH3)2 B. CH3CH2CH=CH2
C. CH2=CH2 D. CH3CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量CaCO3、MgO杂质)生产氢氧化锶的工艺如下:

已知氢氧化锶在水中的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为____。
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12。
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=____。
②若pH过大,将导致氢氧化锶的产率降低,请解释原因____。
(3)“趁热过滤”的目的是____,“滤渣”的主要成分为___。
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为____、过滤、洗涤、干燥。
(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,吸收时的氧化产物为___(填化学式);再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水富县铜锣坝原始森林素有“天然氧吧”之称,其原因是森林空气中富含被称为“空气维生素”的负氧离子,O2— 就是其中一种,其摩尔质量为
A. 33 B. 32 C. 33g﹒mol-1 D. 32g﹒mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学追求减少化工生产对环境造成的污染,下列物质可以称为“绿色氧化剂”的是( )
A.H2O2B.KMnO4C.HNO3D.Ca(ClO)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com