
下列说法正确的是
A.CH3CH2CH2CH3的二氯取代产物只有5种结构
B.油脂的种类很多,但它们水解后都有一相同产物
C.乙烯、苯、纤维素均属于烃类化合物
D.苯和乙烯都能使溴水层褪色,均与溴水发生加成反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B.CaCO3难溶于稀硫酸,也难溶于醋酸
C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-)
D.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求完成下列问题:

 ⑴某有机物的键线式是 请写出它与NaOH溶液反应的化学方程式 ▲ :
⑴某有机物的键线式是 请写出它与NaOH溶液反应的化学方程式 ▲ :
⑵DDT人类合成的第一种有机氯农药,其分子结构球棍模型如
右图所示。请分析该物质的核磁共振1H谱图中有 ▲ 个
 吸收峰。
吸收峰。
 ⑶)F和G( ) 是日常生活中常用的两种合成高分子材料,可由某烃 经下列反应得到。
⑶)F和G( ) 是日常生活中常用的两种合成高分子材料,可由某烃 经下列反应得到。
请回答下列问题:
①F的结构简式为 ▲ 。
②C中所含官能团的名称为 ▲ ,用 ▲ 仪,可以测定D中所含官能团。
③A→B的化学方程式为 ▲ 。

 ④已知 2RCH(OH)COOH 2H2O +
④已知 2RCH(OH)COOH 2H2O +
 请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为 ▲ ,最少用 ▲ 步反应,可以合成产物。
请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为 ▲ ,最少用 ▲ 步反应,可以合成产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1~18号元素的离子aX m+、bY n+、cZP-、dWk-都具有相同的电子层结构,下列关系正确的是
A.若P>K,则还原性cZP- <dWk-
B.若m > n, 则碱性 X(OH)m > Y(OH)n
C.若半径aX m+>bY n+ ,则a<b
D.若半径aX m+ > bY n+ ,则X的单质一定能从含Y n+ 的盐溶液中置换出Y
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E都是短周期元素,原子序数逐渐增大,原子半径按B、A、E、D、C依次增大。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是__________
(2)甲物质的电子式是________ __
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中反应的离子方程式是
(4)用电子式表示A的气态氢化物的形成过程
查看答案和解析>>
科目:高中化学 来源: 题型:
I.(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,该反应的化学方程式为 ;
生成0.1molK2FeO4转移的电子的物质的量 mol 。
。
(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn+2K2FeO4+8H2O  3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时电池的负极反应式为 。充电时电解液的pH (填“增大”“不变”或“减小”)。
II.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH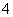 ) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH
) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH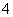 )。
)。
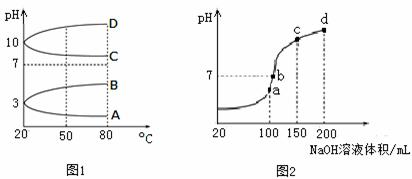
(2)如图1是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母);
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO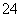 )-c(NH
)-c(NH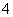 )-3c(Al3+)= mol·L-1。
)-3c(Al3+)= mol·L-1。
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
(4)已知Al(OH)3为难溶物(常温下,Ksp[Al(OH)3]=2.0×10-33)。当溶液pH=5时,某溶液中的Al3+ (填“能”或“不能”)完全沉淀(溶液中的离子浓度小于1×10-5 mol·L-1时,沉淀完全)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:CO(g)  C(s) +
C(s) +  O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
A.低温下是自发变化
B.高温下是自发变化
C.低温下是非自发变化,高温下是自发变化
D.任何温度下都是非自发变化
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,可逆反应2NO2  2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2的同时生成2n mol NO2;
②单位时间内生成n mol O2 的同时生成2n mol NO;
③混合气体的密度不再改变的状态;④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
A.②③⑤⑥ B.①④⑤⑥ C.①③④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
现有五种可溶性物质A、B、C、D、E,它们所含阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO 、CO
、CO 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是________和________(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记为C,当C与B溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕黄色沉淀,向该沉淀中滴入稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为________。
A.SO B.SO
B.SO
C.CH3COO- D.SiO
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的________(填相应的离子符号)。有关反应的离子方程式为___________________。
(4)利用上述已经确定的物质,可以检验出D、E中的阳离子,请简述实验操作步骤、现象及结论:__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com