
现有:
| A.(CH3)3CCH2OH; | B.(CH3)3COH; | C.(CH3)2CHOH; | D. 四种有机物 四种有机物 |
(1)A、D (2)B、C (3)C6H5CH2OOCH和H2O
解析试题分析:醇发生氧化反应时,脱去羟基上的H和与羟基相连的碳原子上的H,即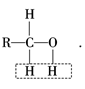
(1)与羟基相连的碳原子上至少含两个氢原子的醇才能被氧化成醛,即: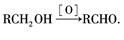
(2)与羟基相连的碳原子上有一个氢原子的醇会被氧化成酮,即: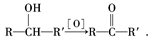
(3)与羟基相连的碳原子上没有氢原子的醇不能被催化氧化。
所以能氧化成醛的是A、D ,氧化成酮的是C,不能被催化氧化是B。
醇的消去反应规律
醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发生消去反应,生成不饱和键。表示为: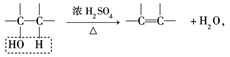
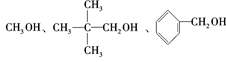 等结构的醇不能发生消去反应。
等结构的醇不能发生消去反应。
所以能消去成烯的是BC,不能消去成烯的是AD。
苯甲醇与甲酸发生酯化反应生成C6H5CH2OOCH甲酸苯甲酯和H2O,故答案为:C6H5CH2OOCH和H2O。
C6H5CH2OH+HCOOH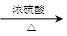 C6H5CH2OOCH+H2O
C6H5CH2OOCH+H2O
考点:考查了醇的化学性质,涉及了催化氧化、消去反应、酯化反应等知识。


科目:高中化学 来源: 题型:填空题
在下列物质中:①K2SO4、②HCHO、③MgSO4、④Hg(NO3)2、⑤NH4Cl、⑥KOH,能使蛋白质变性的是________,能使蛋白质发生盐析的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
乙醇的生产过程可由下图表示:
(1)粉碎玉米的目的是___________________________。
(2)生产过程中为了检验淀粉是否完全水解,可使用的试剂是________。
(3)步骤a的操作是 ( )
| A.蒸发 | B.萃取 | C.蒸馏 | D.分液 |
 nC6H12O6
nC6H12O6 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑查看答案和解析>>
科目:高中化学 来源: 题型:填空题
2004年诺贝尔化学奖授予阿龙.切哈诺沃等三位科学家,以表彰他们发现了泛素调节的蛋白质降解。化合物A是天然蛋白质水解的最终产物,其相对分子质量为165,其中O元素的质量分数小于20%,N元素的质量分数小于l0%。
(1)A的分子式为_______。
(2)光谱测定显示,化合物A分子结构中不存在甲基(-CH3),则化合物A的结构简式为_______ 。
(3)写出A发生缩聚反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有甲、乙、丙三种物质:


甲 乙 丙
(1)关于乙下列叙述正确的是
a.1mol该有机物在加热和催化剂作用下,最多能和2molNaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
① 反应Ⅰ的反应条件是_________________________________________
②其中反应II的化学方程式是
(3)由甲出发合成丙的路线之一如下:
写出反应③的化学方程式__________________________________________________
②写出丙的结构简式_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
I.甲醇是一种可再生燃料,它的沸点为64.7oC。有科学家提出:把含有过量CO2的空气吹入碳酸钾溶液中,然后再把CO2从溶液中提取出来,经化学反应后得到甲醇,其构想流程如下:
试回答下列问题:
(1)写出吸收池中主要反应的化学方程式 。
(2)在2×105pa、300℃合成塔中,若有440gCO2与H2恰好完全反应生成甲醇和水,放出495kJ的热量,试写出合成塔中发生反应的热化学方程式 。
(3)甲醇的一个重要作用是可以制燃料电池,常用KOH作电解质溶液,负极的电极反应式为:
。
Ⅱ.二氧化氯(C1O2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备C1O2的反应原理常采用:2NaC1O3+4HC1=2C1O2↑+C12↑+2H2O+2NaC1。若反应中产生0.1mo1C1O2,则转移电子的物质的量为________mol。
(2)目前已开发出用电解法制取C1O2的新工艺。
①下图示意用石墨做电极,在一定条件下 电解饱和食盐水制取C1O2。写出阳极产生C1O2的电极反应式:____。
②电解一段时间.当阴极产生的气体体积为112mL(标准状况)时,停止电解。
通过阳离子交换膜的阳离子的物质的量为 mol;用平衡移动原理解释阴极区pH增大的原因 。
(3)C1O2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-,现用C1O2将CN-氧化,产物中有两种为气体,其离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C是大家熟悉的与生命活动密切相关的三种化合物,它们所含元素不超过三种,并有下列转化关系:
其中化合物D也是日常生活中常见的化合物,在一定条件下可与单质甲进一步发生如下变化:

回答下列有关问题
(1)在A、B、C、D四种化合中,所含元素相同的是(写物质名称)________、________。
(2)常温下,A和B是通过什么途径转化为C的?____________________________。
(3)目前,化合物B在自然界中的含量呈上升趋势,对环境产生了不良影响,发生这种变化的主要原因是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
食醋的主要成分是乙酸,根据你掌握的知识回答以下有关乙酸的问题。
(1)家用铝制炊具不能储存食醋,说明理由并写出有关反应的化学方程式。
(2)无水乙酸又称冰醋酸(熔点16.6 ℃)。在温度较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将会如何从试剂瓶中取出无水乙酸。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学课外活动小组探究淀粉水解的条件,进行以下两个实验。
(1)实验用品:0.5 g淀粉、4 mL 20%硫酸溶液、氢氧化钠溶液、银氨溶液、碘水。
步骤:在试管1和试管2里各放入0.5 g淀粉,在试管1里加入4 mL 20%硫酸溶液,在试管2里加入4 mL水,都加热3~4 min。用过量碱液中和试管1里的硫酸溶液,把一部分液体倒入试管3。在试管2、3里都加入碘水,观察有没有蓝色出现。在试管1里加入银氨溶液,稍加热后,观察试管内壁上有无银镜出现。
根据所学知识预测可能的实验现象。
实验现象与结论(填入下表):
| 试管 | 加入碘水 | 加入银氨溶液 | 结论 |
| 1 | | | |
| 2 | | | |
| 3 | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com