
【题目】今有常温下两种溶液:① 0.1mol·L-1 NH3·H2O溶液 ② 0.1mol·L-1 NH4Cl溶液。
(1)溶液①的pH_____7(选填 “>”、“<”、“=”),原因是___________________________
(2)溶液②呈_____性(选填 “酸”、“碱”、“中”)原因是____________________________。
(3)关于两种溶液中c(NH4+)的大小叙述正确的是_____(填编号)
a.两种溶液中c(NH4+)都等于0.1mol·L-1
b. 两种溶液中c(NH4+)都小于0.1mol·L-1
c. NH4Cl溶液中c(NH4+)小于NH3·H2O溶液中c(NH4+)
(4)25℃时, 0.1mol/LCH3COOH溶液的pH约为3。向其中加入CH3COONa晶体,待晶体溶解后发现溶液的pH增大。可能的原因有:①_______________;②_______________;为了验证上述哪种解释正确,继续做如下实验:向0.1mol/LCH3COOH溶液中加入少量下列物质中的________(选填字母编号),然后测定溶液的pH。
a.CH3COOK固体 b.CH3COONH4固体 c.NH3 d.NaHCO3固体
(5)25℃时,体积相同,浓度均为0.2mol/L的盐酸和醋酸与镁条反应,开始时两者产生气体的速率盐酸_____(填“大”、“小”或“一样大”),镁条最先消失的是________溶液;如果镁条足量时,选pH相同、等体积的盐酸和醋酸反应,产生气体较多的是________。
【答案】> 氨水是弱碱,电离出氢氧根离子,使得溶液显碱性 酸 氯化铵溶液中铵根离子结合水中氢氧根离子,使得溶液中氢氧根离子浓度小于氢离子浓度,溶液显酸性 b 醋酸钠水解,溶液呈碱性,增大了c(OH-),因而溶液的pH增大 醋酸钠溶于水电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大 b 大 盐酸 醋酸
【解析】
(1)氨水是弱碱,在水溶液能电离出氢氧根离子,导致氢氧根离子浓度大于氢离子浓度;
(2)氯化铵是强酸弱碱盐,能水解导致溶液中氢离子浓度大于氢氧根离子浓度;盐类水解反应是吸热反应,升高温度能促进水解;
(3)氨水是弱电解质,在水中电离程度很小;氯化铵是强酸弱碱盐,能水解但水解程度很小,主要以电离为主,据此分析铵根离子浓度大小;
(4)0.1mol/LCH3COOH溶液的pH约为3,说明醋酸为弱酸,在醋酸溶液中存在电离平衡CH3COOH ![]() H++CH3COO-。向其中加入CH3COONa晶体,溶液的pH增大,可能是:①醋酸钠水解,溶液呈碱性,②醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离;要验证哪种正确,不能加入碱性物质,只能加入中性物质,据此分析判断;
H++CH3COO-。向其中加入CH3COONa晶体,溶液的pH增大,可能是:①醋酸钠水解,溶液呈碱性,②醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离;要验证哪种正确,不能加入碱性物质,只能加入中性物质,据此分析判断;
(5)相同温度,相同浓度的盐酸和醋酸,盐酸溶液中氢离子浓度大于醋酸溶液中氢离子浓度;pH相同、等体积的盐酸和醋酸,醋酸的物质的量大于盐酸的物质的量,据此分析解答。
(1)氨水是弱碱,在水溶液能电离出氢氧根离子,导致氢氧根离子浓度大于氢离子浓度,溶液呈碱性,溶液的pH>7,电离方程式为:NH3H2ONH4++OH-,故答案为:>;氨水是弱碱,电离出氢氧根离子,使得溶液显碱性,NH3H2ONH4++OH-;
(2)氯化铵是强酸弱碱盐,铵根离子结合水中氢氧根离子发生水解,使得溶液中氢氧根离子浓度小于氢离子浓度,溶液呈酸性,故答案为:酸;氯化铵溶液中铵根离子结合水中氢氧根离子,使得溶液中氢氧根离子浓度小于氢离子浓度,溶液显酸性;
(3)氨水是弱电解质,在水中电离程度很小;氯化铵是强酸弱碱盐,能水解但水解程度很小,主要以电离为主,所以相同浓度的氨水和氯化铵溶液,氯化铵溶液中铵根离子浓度较大,但都小于0.1mol/L,故选b;
(4)0.1mol/LCH3COOH溶液的pH约为3,说明醋酸为弱酸,醋酸溶液中存在电离平衡CH3COOH ![]() H++CH3COO-。向其中加入CH3COONa晶体,待晶体溶解后发现溶液的pH增大,可能的原因有:①醋酸钠水解,溶液呈碱性,增大了c(OH-),因而溶液的pH增大,②醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大;CH3COONH4溶液中,CH3COO-和NH4+都发生水解,且水解程度相等,CH3COONH4溶液呈中性,将CH3COONH4固体加入到0.1 molL-1醋酸中,如pH增大,说明CH3COO-抑制了醋酸的电离,其它物质的水溶液都呈碱性,加入后,溶液的pH一定会增大,不能用于证明,故答案为:醋酸钠水解,溶液呈碱性,增大了c(OH-),因而溶液的pH增大;醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大;b;
H++CH3COO-。向其中加入CH3COONa晶体,待晶体溶解后发现溶液的pH增大,可能的原因有:①醋酸钠水解,溶液呈碱性,增大了c(OH-),因而溶液的pH增大,②醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大;CH3COONH4溶液中,CH3COO-和NH4+都发生水解,且水解程度相等,CH3COONH4溶液呈中性,将CH3COONH4固体加入到0.1 molL-1醋酸中,如pH增大,说明CH3COO-抑制了醋酸的电离,其它物质的水溶液都呈碱性,加入后,溶液的pH一定会增大,不能用于证明,故答案为:醋酸钠水解,溶液呈碱性,增大了c(OH-),因而溶液的pH增大;醋酸钠溶于水,电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大;b;
(5)相同温度,相同浓度的盐酸和醋酸,盐酸溶液中氢离子浓度大于醋酸溶液中氢离子浓度,所以开始时,盐酸的反应速率大于醋酸的反应速率,反应过程中盐酸的反应速率一直大于醋酸,则镁条最先消失的是盐酸;如果镁条足量时,选pH相同、等体积的盐酸和醋酸,醋酸的物质的量大于盐酸的物质的量,与足量镁条反应,生成氢气较多的是醋酸;故答案为:大;盐酸;醋酸。


科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组模拟上述过程,所设计的装置如图所示:
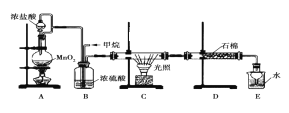
(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③_______________________。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_______________________。
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、某温度时,在一个 10L 的恒容容器中,X、Y、Z 均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
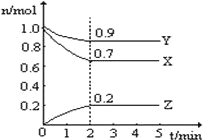
(1)该反应的化学方程式为:________________________。
(2)反应开始至 2min,以气体 Z 表示的平均反应速率为:____________________。
(3)将 a mol X 与 b mol Y 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中 a∶b=________。
Ⅱ、在恒温恒容的密闭容器中,当下列物理量不再发生变化时:
①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(1)一定能证明2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是 __________________填序号,下同)。
(2)一定能证明 I2(g)+H2(g)2HI(g)达到平衡状态的是____________________。
(3)一定能证明 A(s)+2B(g)C(g)+D(g)达到平衡状态的是_________________(B、C、D 均无色)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机乙偶姻存在于啤酒中,是酒类调香中一个极其重要的品种,某研究性学习小组为确定乙偶姻的结构,进行如下探究。
步骤一:将乙偶姻蒸气通过热的氧化铜(催化剂)氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收,如图1。2.64 g乙偶姻的蒸气氧化产生5.28 g二氧化碳和2.16 g水。
步骤二:升温使乙偶姻汽化,测其密度是相同条件下H2的44倍
步骤三:用核磁共振仪测出乙偶姻的核磁共振氢谱如图2,图中4个峰的面积比为1∶3∶1∶3。
步骤四:利用红外光谱仪测得乙偶姻分子的红外光谱如图3。



(1)图1装置中两支U型管不能互换的理由是__________________________.
(2)乙偶姻的摩尔质量为____________。
(3)乙偶姻的分子式为____________________。
(4)乙偶姻的结构简式为 ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请参照元素①-⑧在表中的位置,根据判断出的元素回答问题:
① | |||||||
② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ |
(1)⑧原子的最外层电子的轨道表达式为___________________,关于它的最外层p亚层电子的说法错误的是_________。(填序号)
a. 能量相同 b.电子云形状相同
c. 自旋方向相同 d. 电子云伸展方向相同
(2)③和①组成的四核分子的化学式为___________,空间构型为_____________,属于_____分子(填“极性”或“非极性”)。
(3)比较④、⑤元素常见离子的半径大小(用化学式表示)______>_____;②、③ 两元素非金属性较强的是 ______(写元素符号),写出证明该结论的一个事实:___________________________ 。
(4)④、⑤元素形成的四原子化合物的电子式为 ___________ ;已知⑥元素的氧化物的熔点为2054℃,且以它为原料,可以通过电解的方法得到铝,据此推断⑥元素的氧化物为_________晶体(填“分子晶体”或“离子晶体”或“原子晶体”或“金属晶体”)。⑥元素的氧化物熔点______⑥元素的氯化物熔点(填“大于”“小于”“等于”),请解释其原因______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(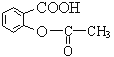 )能解热镇痛。
)能解热镇痛。
(1)阿司匹林属于__________(填“无机化合物”或“有机化合物”)。
(2)阿司匹林中含氧官能团有酯基和__________(填名称)。
(3)向阿司匹林的水溶液中滴入2~3滴紫色石蕊溶液,溶液颜色变红,说明阿司匹林溶液具有________性。
(4)根据阿司匹林的结构推断它能够发生的化学反应类型为________(填序号)。
①中和反应 ②加成反应 ③取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用。
(1)真空碳热还原![]() 氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g)△H=akJmol-1
3AlCl(g)=2Al(l)+AlCl3(g)△H=bkJmol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=________ kJmol-1用含a、b的代数式表示![]() ;
;
(2)用活性炭还原法可以处理氮氧化物![]() 某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)N2(g)+CO2(g)△H=QkJmol-1在T1℃时,反应进行到不同时间测得各物质的浓度如下:
某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)N2(g)+CO2(g)△H=QkJmol-1在T1℃时,反应进行到不同时间测得各物质的浓度如下:
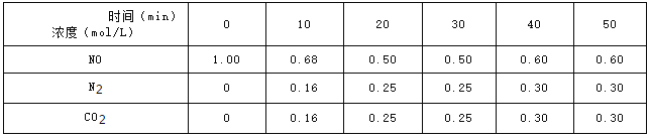 ①
①![]() 内,NO的平均反应速率
内,NO的平均反应速率![]() _________,
_________,![]() 时,该反应的平衡常数
时,该反应的平衡常数![]() _________;
_________;
②30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 ___________ ![]() 填字母编号
填字母编号![]() .
.
![]() 通入一定量的NO b.加入一定量的活性炭
通入一定量的NO b.加入一定量的活性炭
![]() 加入合适的催化剂
加入合适的催化剂 ![]() 适当缩小容器的体积
适当缩小容器的体积
③若30min后升高温度至![]() ,达到平衡时,容器中NO、N2、CO2的浓度之比为3∶1∶1,则Q____________
,达到平衡时,容器中NO、N2、CO2的浓度之比为3∶1∶1,则Q____________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() .
.
④在恒容条件下,能判断该反应一定达到化学平衡状态的依据是 ________填选项编号
![]() .
.
![]() 单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的温度不再发生改变
![]() 混合气体的密度不再发生改变
混合气体的密度不再发生改变
![]() 反应体系的压强不再发生改变
反应体系的压强不再发生改变
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示:
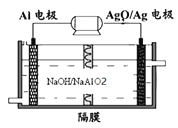
请写出该电池正极反应式__________常温下,用该化学电源和惰性电极电解300mL硫酸铜溶液(过量),消耗27mgAl,则电解后溶液的![]() ___________
___________![]() 不考虑溶液体积的变化
不考虑溶液体积的变化![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%,质量分数),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO47H2O的工艺流程如下:
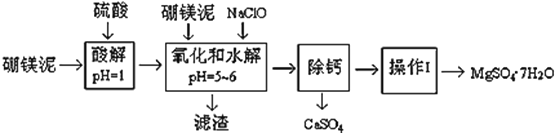
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,量取浓硫酸需要使用量筒的规格为__________(填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl ,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有__________,___________。
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法___________________。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤______。“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,______,便得到了MgSO47H2O
(6)实验中提供的硼镁泥共100 g,得到 MgSO47H2O为172.2 g ,则MgSO47H2O 的产率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对已达化学平衡的反应:2X(g)+Y(g)![]() 2Z(g),减小压强后,对反应产生的影响是
2Z(g),减小压强后,对反应产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正反应速率先减小后增大,逆反应速率减小,平衡向逆反应方向移动
D.逆反应速率先减小后增大,正反应速率减小,平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com