
【题目】三氯化磷是一种无色液体,熔点-93.6℃,沸点76.1℃,PCl3遇到水蒸气剧烈反应。实验室利用下列装置制备三氯化磷。

(1)仪器W的名称是______________,其作用是______________________________。
(2)盛P2O5的长玻璃管的作用是___________,浓硫酸的作用是_____。
(3)实验室用KMnO4与浓盐酸制取氯气的离子方程式为________________________。
(4)氯气通入烧瓶中会发生燃烧,说明P4与Cl2反应的△H____0(填“>”或“<”)。
(5)烧瓶中得到的产物除PCl3外还可能含有______(填化学式),进一步精制的方法是________。
(6)PCl3与H2O反应的化学方程式为________________________________________。
【答案】 (直型)冷凝管 冷凝回流 防止空气中的水蒸气进入反应器 干燥氯气 2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O < PCl5 蒸馏 PCl3+3H2O=H3PO3+3HCl
【解析】(1)仪器W的名称是(直型)冷凝管,其作用是冷凝回流;
(2) PCl3遇到水蒸气剧烈反应,盛P2O5的长玻璃管的作用是防止空气中的水蒸气进入反应器与三氯化磷反应,浓硫酸的作用是干燥氯气,防止产生的三氯化磷与水反应;(3)实验室用KMnO4与浓盐酸反应制取氯气,同时生成氯化钾、氯化锰和水,其离子方程式为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;(4)因白磷遇氯气发生燃烧,燃烧反应都是放热反应,说明P4与Cl2反应的△H<0;(5)由于发生反应PCl3+Cl2=PCl5(固),会有五氯化磷溶解其中,依据三氯化磷沸点,对其进行蒸馏提纯;(6)依据氯显-1价,水解时用-OH替代氯,故得H3PO3和HCl,则反应为:PCl3+3H2O=H3PO3+3HCl。


科目:高中化学 来源: 题型:
【题目】有机物F( )是合成某种药物的中间体,它的一种合成路线如下:
)是合成某种药物的中间体,它的一种合成路线如下:
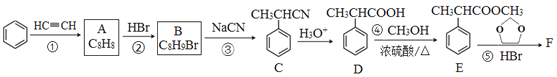
回答下列问题:
(1)A的结构简式为______,分子中处于同一平面的原子最多有____个。
(2)E中官能团名称是_____,①~④中属于加成反应的是_______(填序号)。
(3)反应③的化学方程式为______________。
(4)反应⑤的生成物有两种,除了F以外,另一种生成物的名称是______。
(5)满足下列条件的D的同分异构体有______种。
①能与FeCl3溶液发生显色反应; ②能发生银镜反应; ③分子中有1个甲基
(6)仿照E的合成路线,设计一种由![]() 合成
合成![]() 的合成路线_________________。
的合成路线_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题.
成分 | 质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 68.4 | 342 |
硫酸钾 | 0.50 | 174 |
阿司匹林 | 0.35 | 180 |
高锰酸钾 | 0.50 | 158 |
硝酸银 | 0.04 | 170 |
(1)“鲜花保鲜剂”中蔗糖的物质的量浓度为 .
(2)配制该500mL“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有: .
(3)在溶液配制过程中,下列操作能使配制结果偏小的是 .
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.移液时,液体不小心从外壁流出
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
E.用托盘天平称量蔗糖时,左盘放砝码,右盘放蔗糖.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C和H2在生产、生活、科技中是重要的燃料。
①2C(s)+O2(g)= 2CO(g) △H=-220kJ/mol
②
下列推断正确的是( )
A. C(s)的燃烧热110kJ/mol
B. 2H2 (g) +O2 (g) =2H2O (g) △H=+480kJ/mol
C. C(s) +H2O(g)==CO(g) +H2 (g) △H=-220kJ/mol
D. 分解2molH2O(1),至少需要4×462kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,5.6L甲烷和乙烯的混合气体中含氢原子数为NA
B. 1L 0.2mol·L-1NaHCO3溶液中含Na+数为0.2NA
C. 4.6g钠用铝箔包裹并刺小孔,与足量水充分反应生成氢气分子数为0.1NA
D. 反应NH4Cl+NaNO2![]() N2↑+NaCl+2H2O,每生成0.1mol N2,转移电子数为0.6NA
N2↑+NaCl+2H2O,每生成0.1mol N2,转移电子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《太平惠民和剂局方》中对精制蜡的过程有如下记载:“……先将蜡六两熔化作汁,以重绵滤去滓,以好酒一升,于银石器内煮蜡熔,数沸倾出,候酒冷,其蜡自浮,取蜡称用。”文中涉及的操作方法是( )
A. 萃取B. 升华C. 重结晶D. 渗析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁制容器盛装冷的浓硫酸.为研究铁制材料与热的浓硫酸的反应,某学习小组进行了以下探究活动.
(1)【探究一】
Ⅰ.将已除去表面氧化物的铁钉(碳素钢)放入冷的浓硫酸中,10min后投入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 .
Ⅱ.另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
①甲同学认为X中除Fe3+外还可能含有Fe2+ . 若要确认其中是否含有Fe2+ , 应选用(填序号).
a.KSCN溶液和新制氯水
b.铁粉和KSCN溶液
c.浓氨水
d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O═2HBr+H2SO4 , 然后加入足量BaCl2溶液,经适当操作后,得2.33g干燥固体.由此推知气体Y中SO2的体积分数为 .
(2)【探究二】
分析上述实验中所得SO2的体积分数,丙同学认为气体Y中还可能含有H2和Q气体.为此设计了如图所示的探究实验装置(图中夹持仪器已省略).
①装置B中试剂的作用是 .
②认为气体Y中还可能含有Q的理由是(用化学方程式表示).
③为确认Q的存在,需添加装置M于(填序号).
a.装置A之前 b.装置A、B间
c.装置B、C间 d.装置C、D间
④如果气体Y中含有H2 , 实验现象应是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厨房垃圾发酵液可通过电渗析法处理,同时得到乳酸。原理如图所示(图中HA表示乳酸分子,A-表示乳酸根离子,乳酸的摩尔质量为90g/mol,下列有关说法中正确的是( )

A. 电极a为阴极,放出H2
B. 通电一段时间后,硫酸溶液的pH升高
C. A-通过阴离子交换膜从阴极进入浓缩室
D. 对400mLl0g/L乳酸溶液通电后,当外电路通过0.5mole-时浓度,上升为145g.L-1(溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的单质及其化合物在工农业生产和生活中有重要的作用。用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO (g)![]() N2(g)+CO2(g) △H= QkJ/mol。
N2(g)+CO2(g) △H= QkJ/mol。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:

(1)0~10min内,NO的平均反应速率V(NO)=______,T1℃,该反应的平衡常数K=________;
(2) 30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是______.(填字母编号)。
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
(3)若30 min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q_____0(填“>”或“<")。
(4)在恒容条件下,能判断该反应一定达到化学平衡状态的依据是______(填选项编号)。
a.单位时间内生成2nmol NO (g)的同时消耗nmol CO2(g) b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变 d.反应体系的压强不再发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com