
����Ŀ���� NA Ϊ�����ӵ�������ֵ������˵����ȷ����
A.��״���£�1 L ������ȫȼ�պ������ɵ���̬����ķ�����Ϊ![]() NA
NA
B.10 g 46%���Ҵ���Һ����ԭ�ӵĸ���Ϊ 0.6 NA
C.28 g ��ϩ���ϩ�Ļ�����壬���õĵ��Ӷ���Ϊ 6 NA
D.100 mL 0.1 mol/L CH3COOH ��Һ�������Ҵ���Ũ���Ṳ�ȣ�����������Ӧ������������������ ��Ϊ 0.01 NA
���𰸡�C
��������
A����״���£�����ΪҺ�壬��������22.4L/mol����ȼ�ղ���ķ�������A����ȷ��
B��10 g 46%���Ҵ���Һ����ԭ�ӵĸ���Ϊ![]() =1.2 NA��B����ȷ��
=1.2 NA��B����ȷ��
C��28 g��ϩ��28 g��ϩ�У����õ��Ӷ�����Ϊ6 NA����28 g��������У����õĵ��Ӷ���ҲӦΪ6 NA��C��ȷ��
D��������ӦΪ���淴Ӧ������100 mL 0.1 mol/L CH3COOH��Һ�������Ҵ���Ũ���Ṳ�ȣ�������������������С��0.01 NA��D����ȷ��
��ѡC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪ����ֱ��ˮ�Ϸ�����ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ[����n(H2O)��n(C2H4)��1��1]
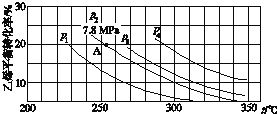
����ʽ������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��Kp��__(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)��
��ͼ��ѹǿ(p1��p2��p3��p4)�Ĵ�С˳��Ϊ___��������___��
������ֱ��ˮ�Ϸ������õĹ�������Ϊ������/������Ϊ��������Ӧ�¶�290�棬ѹǿ6.9MPa��n(H2O)��n(C2H4)��0.6��1����ϩ��ת����Ϊ5%����Ҫ��һ�������ϩת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬���ɲ�ȡ�Ĵ�ʩ��___��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ǻ�ѧ�о��Ļ������������и�ʵ��װ��ͼ��������ȷ����( )
|
|
|
|
�� | �� | �� | �� |
A.װ�â�����Һ�ϲ���ɫ���²��Ϻ�ɫB.װ�âڿ���������HCl���壬����ֹ����
C.װ�âۿ�������ȡ����ˮD.װ�â���Һ�����ɺ�ֹͣ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����к�������̼ԭ�ӵ���
A.CF2Cl2B.![]()
C.CH3CH2CHClCH2CH2CH3D.CH2�TCH-COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ�������[Fe(OH)SO4]n��������ˮ��(������)�������̷�(FeSO47H2O)��KClO3��ˮ��Һ�з�Ӧ�õ�������˵������ȷ���ǣ� ��
A.KClO3����������ÿ����1mol[Fe(OH)SO4]n����![]() molKClO3
molKClO3
B.���ɾۺ���������ˮ��Һ��pH����
C.�ۺ�����������ˮ��Һ��ˮ���������������������ˮ
D.�ڷ�Ӧ���������ͻ�ԭ�����ʵ���֮��Ϊ1��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽��ľ̿��ŨH2SO4��Ӧ�IJ������Ƿ����CO2��ijͬѧѡ����ͼ��ʾװ�ý���ʵ�飺
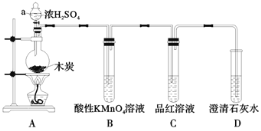
��1����װ������ʵ��װ�ú���װ��ҩƷ֮ǰ�����ʵ�������__��
��2��д��A�з�����Ӧ�Ļ�ѧ����ʽ___��
��3��װ��B�������dz�ȥ�����е�SO2�������ķ�ӦΪ MnO4-+ SO2+ H2O= Mn2++ SO42-+ H+����ƽ�÷�Ӧ����ʽ___����������KMnO4��Һ���ձ����22.4LSO2����Ӧת�Ƶĵ�����Ϊ___��
��4��װ��C��������__��
��5�������ʵ���Ũ��Ϊ18.4mol/L��Ũ��������500mL0.5mol/L��ϡ���ᣬ��Ҫ��������Ͳ���ձ�������������ͷ�ι��⣬����Ҫ__������ʱ�������ӿ̶��ߣ����������ҺŨ�Ȳ�����Ӱ��Ϊ__���ƫ����ƫС������Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ؼ� ~ �������ڱ��е�λ�������ʾ������˵��������ǣ� ��
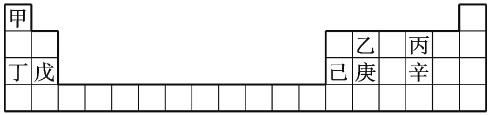
A.Ԫ�ؼס�������ĵ��ʶ��ǽ���
B.Ԫ���ҡ����������Ƿǽ���Ԫ��
C.Ԫ���ҡ������������γ�������
D.����������ȿ�����![]() ��Һ�ֿ�����ϡ����
��Һ�ֿ�����ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ԭ�ԣ�Fe2����Br������100mLFeBr2��Һ��ͨ��3.36L(��״��)Cl2����Ӧ�����Һ��Cl����Br�������ʵ���Ũ����ȣ���ԭ��Һ��FeBr2�����ʵ���Ũ��Ϊ(����)
A. 2 mol��L��1 B. 1.5 mol��L��1 C. 1 mol��L��1 D. 0.75 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ2.0 L�ĺ����ܱ������з�����Ӧ��PCl5(g)![]() PCl3(g)+Cl2(g)��
PCl3(g)+Cl2(g)��
��� | �¶� /�� | ��ʼ���� ����/mol | ƽ������ ����/mol | �ﵽƽ�� ����ʱ��/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
�� | 320 | 0.40 | 0.10 | 0.10 | t |
�� | 320 | 0.80 | t1 | ||
�� | 410 | 0.40 | 0.15 | 0.15 | t2 |
����˵����ȷ����
A.ƽ�ⳣ��K��������>������
B.��Ӧ����ƽ��ʱ��PCl5��ת���ʣ�������>������
C.��Ӧ����ƽ��ʱ���������е�ƽ������Ϊv(PCl5)=![]() mol��L-1��s-1
mol��L-1��s-1
D.��ʼʱ���������г���PCl5 0.30 mol��PCl3 0.45 mol��Cl2 0.10 mol����Ӧ�����淴Ӧ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com