
【题目】某溶液中存在大量的H+、Cl一、SO42一,该溶液中还可能大量存在的是
A. HCO3一 B. Ba2+ C. Al3+ D. Ag+
科目:高中化学 来源: 题型:
【题目】下列各组物质充分反应后过滤,将滤液加热、蒸干至质量不变,最终不能得到纯净物的是( )
A. 向含1 mol Ca(HCO3)2的溶液中加入1 mol Na2O2
B. 向带有氧化膜的铝片中加入盐酸
C. 向漂白粉溶液中通入过量CO2
D. 向含1 mol KAl(SO4)2的溶液中加入2 mol Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应中的能量变化,下列说法中不正确的是( )
A. 燃烧反应都是放热反应
B. 对于可逆反应:aA(g)+bB(g)![]() bC(g)+dD(g),如果正反应放热,逆反应一定吸热
bC(g)+dD(g),如果正反应放热,逆反应一定吸热
C. 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量
D. 只有放热的氧化还原反应才可以设计为原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() (△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:

回答问题:
⑴反应的化学方程式中a∶b∶c为;
⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为;
⑶B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是,其值是;
⑷由第一次平衡到第二次平衡,平衡移动的方向是,采取的措施是;
⑸比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2T3(填“<”“>”“=”)判断的理由是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃下,部分弱酸的电离常数如表。下列有关说法不正确的是

A. 若 HCOONa和 HCOOH的混合溶液的pH=3,则c(HCOOH)/c(HCOO-)=10
B. 相同浓度的 HCOONa和 NaClO溶液中离子总浓度前者大
C. 任何浓度NaHS溶液中总存在:c(H2S)+c(H+)=c(OH-)+c(S2-)
D. 向 NaClO溶液中通入H2S发生的反应为2C1O-+H2S===S2-+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化亚铜(CuⅠ)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜的流程。
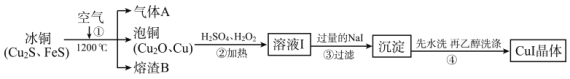
(1)FeS中S的化合价为_____________。
(2)步骤①中Cu2S被转化为Cu,同时有大气污染物A生成,相关化学反应方程式为_____________,熔渣B的主要成分为黑色磁性物质,其化学式为_____________。
(3)步骤②中H2O2的作用是_____________;步骤③中加入过量NaI涉及的主要离子反应方程式为_____________。
(4)步骤④用乙醇洗涤的优点是_____________;检验沉淀是否洗涤干净的方法是_____________。
(5)溶液I中通常含少量Fe(Ⅲ)。已知该工业条件下,Fe(OH)3的Ksp=1.0×10-38,据此分析除去Fe(Ⅲ)(即c(Fe3+)≤1.0×10-5mol/L)应调节pH不小于_____________(水的离子积以常温计)。
(6)准确称取 m g CuI样品,加入足量的Fe2(SO4)3溶液,发生反应为2CuⅠ+4Fe3+===2Cu2++4Fe2++I2,待样品完全反应后,用amol/L酸性KMnO4溶液滴定Fe(Ⅱ),消耗标准液的体积平均值为ⅴmL。样品中CuI的质量分数的计算表达式为_____________;如果滴定前,酸式滴定管没有用标准液润洗,CuI的质量分数_____________(填“偏低”、“偏高”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为原料合成1,4 —己二醇的路线示意图如下:

(1)有机化合物![]() 中官能团的名称为__________________________________。
中官能团的名称为__________________________________。
(2)反应⑤需要的试剂和条件是_______________;反应类型是_______________________。
(3)有机化合物C的结构简式是_________________________。
(4)写出反应①、③、⑧的化学方程式:① __________________;③ ___________________;
⑧ ________________________。
(5)在反应①~⑧中属于取代反应的有______________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL密度为1.84g/cm3,质量分数为98%的浓硫酸中,c(H2SO4)是( )
A. 18.4 B. 9.8mol·L—1 C. 1.84mol·L—1 D. 18.4mol·L—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组用高锰酸钾粉末与浓盐酸制取氯气,并验证其性质。

(资料在线)高锰酸钾粉末与浓盐酸混合即产生氯气。
请回答下列问题:
(1)该实验中A部分的装置应选用下图中的______(填序号)

(2)实验中A发生反应的离子方程式是_________。
(3)一段时间后D中的现象为_________。
(4)请你设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤) _________。
(5)图(1)整套实验装置存在的明显缺陷是_________。
(6)图(2)装置a处通入氯气,证明氯气是否具有漂白性,该设计能否达到实验目的? _________ (填“能”或“不能”)。若能请说明理由,若不能则提出改进的措施_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com