
【题目】25℃下,部分弱酸的电离常数如表。下列有关说法不正确的是

A. 若 HCOONa和 HCOOH的混合溶液的pH=3,则c(HCOOH)/c(HCOO-)=10
B. 相同浓度的 HCOONa和 NaClO溶液中离子总浓度前者大
C. 任何浓度NaHS溶液中总存在:c(H2S)+c(H+)=c(OH-)+c(S2-)
D. 向 NaClO溶液中通入H2S发生的反应为2C1O-+H2S===S2-+2HClO
【答案】D
【解析】
由表给电离常数可知,电离程度由大到小的顺序为:HCOOH>H2S> HClO>HS—,则对应离子的水解程度大到小的顺序为:S2-> C1O-> HS—> HCOO-,注意NaClO具有强氧化性,与H2S在溶液中发生氧化还原反应,不能发生复分解反应。
A项、在溶液中HCOOH的电离常数Ka=![]() ,则pH=3的HCOONa和 HCOOH的混合溶液中
,则pH=3的HCOONa和 HCOOH的混合溶液中![]() =10,故A正确;
=10,故A正确;
B项、HCOONa溶液中电荷守恒关系为:C(Na+)+C(H+)=C(OH-)+c(HCOO-),溶液中离子总数为2×[c(Na+)+c(H+)]×V,同理可得NaClO溶液中总数为2×[c(Na+)+c(H+)]×V,由电离常数可知HCOOH比HCN易电离,则等体积、等浓度的HCOONa和NaClO溶液中,ClO—水解程度更大,溶液中的c(OH—)大、c(H+)小,所以HCOONa溶液中离子总数大于NaClO溶液,故B正确;
C项、NaHS溶液中一定存在质子守恒关系:c(H2S)+c(H+)=c(OH-)+c(S2-),故C正确;
D项、向 NaClO溶液中通入H2S,因NaClO具有强氧化性,与H2S在溶液中发生氧化还原反应,不能发生复分解反应,故D错误。
故选D。


科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g) ![]() CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
D. 对于反应2HI(g) ![]() H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是
A. 过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑
B. 向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH- =2Al(OH)3↓+3BaSO4↓
C. 用铜做电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D. FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的电离方程式书写正确的是( )
A. FeSO4=Fe3++SO42— B. Ca(OH)2=Ca2++2(OH)—
C. H2SO4= 2H++ SO42— D. KClO3=K++Cl—+O2—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸(![]() )又名草酸,是生物体的一种代谢产物;现设计如下实验探究草酸分解反应的产物。
)又名草酸,是生物体的一种代谢产物;现设计如下实验探究草酸分解反应的产物。
资料查阅:
Ⅰ.草酸熔点为102℃,150~160℃升华,157℃时开始分解。在人体中C2O42-容易与钙离子形成草酸钙导致肾结石。
Ⅱ.PdCl2溶液可用于检验CO,反应的化学方程式为CO+PdCl2+H2O====CO2+2HCl+Pd(黑色粉末)。
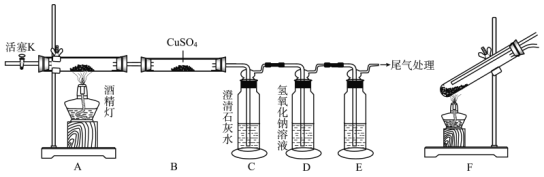
(1)A中盛放草酸的玻璃仪器的名称是_____________,实验中观察到B中CuSO4粉末变蓝,相关化学方程式为_____________。
(2)装置E中的试剂为_____________,当观察到_____________(填现象),可以证明有CO气体生成。
(3)下面是该实验过程中的相关操作,正确的操作顺序为_________(填入下列步骤的字母)。
A.向装置中通入适量N2 B.点燃酒精灯 C.检查装置气密性
D.装入相关试剂 E.再次通入N2并熄灭酒精灯
(4)为准确证眀A有CO2气体产生,需取少量C中沉淀于试管中,滴加过量盐酸并观察是否有气泡产生,其目的是_____________,草酸分解反应的化学方程式为_____________。
(5)实验过程中,学生提出装置A应改为装置F,请结合信息分析其原因是_____________;如果草酸粉末溅入眼睛里,应立即_____________,然后就医。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近两年流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为![]() ,下列说法不正确的是
,下列说法不正确的是
A. 苹果酸在一定条件下能发生酯化反应
B. 苹果酸在一定条件下能发生催化氧化反应
C. 苹果酸在一定条件下能发生取代反应
D. 1 mol苹果酸与Na2CO3溶液反应最多消耗1 mol Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com