
| A、H+、AlO2-、NO3-、Cl- |
| B、MnO4-、H+、K+、NO3- |
| C、Ba2+、Na+、HCO3-、OH- |
| D、K+、SO42-、S2-、Na+ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、60g水晶晶体中,含有“Si-O”键的数目为2NA |
| B、14g氮气含有π键数为2NA |
| C、18g冰中含有的氢键数目为2NA |
| D、12g金刚石中含有C-C键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾净水的原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、硫酸铝溶液与硫化钠溶液混合:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑ |
| C、碳酸钠溶液呈碱性的原因:CO32-+2H2O?H2CO3+2OH- |
| D、FeCl3溶液加入碳酸氢钠溶液中:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
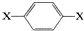 ,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )
,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )| A、该有机物不可能为芳香醇 |
| B、该有机物的分子式可能为C8H10O2 |
| C、该有机物可能与NaOH溶液反应 |
| D、该有机物可能与溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
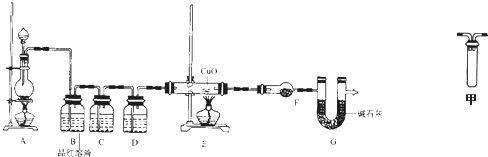
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com