
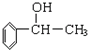
 (1)苏合香醇可以用作食用香精,其结构简式如图所示.
(1)苏合香醇可以用作食用香精,其结构简式如图所示.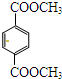 的同分异构体有多种,满足下列条件的共有
的同分异构体有多种,满足下列条件的共有 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置.
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置. 的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,
的同分异构体有多种,满足①苯环上只有两个取代基,②1mol 与足量的NaHCO3溶液反应生成2mol CO2气体,则含2个-COOH,2个取代基分别为-COOH、CH2CH2COOH,或-COOH、-CH(CH3)COOH,或-CH2COOH、-CH2COOH,或-CH3、-CH(COOH)2,均存在邻、间、对三种位置,则同分异构体的数目为4×3=12种,

科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
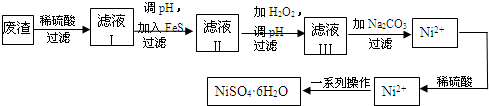
 铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是
有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 加入试剂 | 操作方法 |
| ①粗苯甲酸的提纯 | ||
| ②乙醇(水) | ||
| ③乙酸乙酯(乙酸) | ||
| ④乙烷(乙烯) | ||
| ⑤苯(酒精) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,48gO3气体含有NA个O3分子 |
| B、标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
| C、1L0.5mol?L-1Na2CO3溶液中含有0.5NA个CO32- |
| D、标准状况下,33.6LH2O含有1.5NA个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不需要通过化学反应就能从海水中获得食盐和淡水 |
| B、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| C、高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害 |
| D、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B元素组成的一种单质具有漂白性,能使KMnO4溶液紫色褪去 |
| B、B、D两种元素形成的一种化合物也具有一定的漂白性,能使紫色石蕊紫色褪去 |
| C、C元素分别与A元素和B元素形成的化合物都是离子晶体,一定均与水反应生成强碱和无色气体 |
| D、A2B的热稳定性强于A2D、沸点也高于A2D,但解释的理由不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、维生素在天然食品中含量丰富,所以加工后的食品中维生素含量也高 |
| B、人体细胞中的酸碱平衡是不能通过选择食物调节的 |
| C、为了食品安全,我国应该禁止使用食品防腐剂 |
| D、食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com