
 (1)如图为牺牲阳极的阴极保护法的实验装置,此装置中Zn电极上的电极反应为
(1)如图为牺牲阳极的阴极保护法的实验装置,此装置中Zn电极上的电极反应为

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 石墨晶体是层状结构,在每一层内;每一个碳原于都跟其他3个碳原子相结合,如图是其晶体结构的俯视图,则如图中7个六元环完全占有的碳原子数是( )
石墨晶体是层状结构,在每一层内;每一个碳原于都跟其他3个碳原子相结合,如图是其晶体结构的俯视图,则如图中7个六元环完全占有的碳原子数是( )| A、10个 | B、14个 |
| C、18个 | D、21个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将烧碱逐滴加入醋酸溶液中至溶液呈中性,则该混合液中还有少量醋酸未被中和 |
| B、将0.1 mol?L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、H+浓度都逐渐增大 |
| C、将醋酸逐滴加入醋酸钠溶液中至溶液呈酸性,则该溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、常温下,将pH=12的烧碱溶液与pH=2的醋酸溶液等体积混合,所得混合液的pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的pH值:②>③>① |
| B、水电离出的c(OH-):③>①>② |
| C、①和②等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)=0.05mol/L |
| D、室温,碳酸钙在①中的ksp比在水中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强度跟铝相比有很大的提高,在某些性能上相当于钢材 |
| B、密度较小,只有钢材的三分之一左右,适用于做飞行器、火箭、卫星、导弹等 |
| C、熔点和铝相比有一定的提高,常被用于制造家庭使用的炊具 |
| D、抗腐蚀性能较强,常被建筑行业用作材料以及门窗框架 |
查看答案和解析>>
科目:高中化学 来源: 题型:
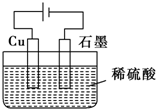
| A、电解过程中,铜电极上有H2产生 | ||||
B、电解初期,总反应方程式为 Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,H+的浓度不断减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
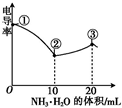 电导率是衡量电解质溶液导电能力大小的物理量.室温下,用0.100mol?L-1的NH3?H2O 滴定10.00mL浓度均为0.100mol?L-1 的HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量.室温下,用0.100mol?L-1的NH3?H2O 滴定10.00mL浓度均为0.100mol?L-1 的HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )| A、①点溶液中:c(H+)=0.200 mol?L-1 |
| B、溶液温度:①>③>② |
| C、③点溶液中:c(Cl-)>c(CH3COO-) |
| D、③点后因离子数目减少使溶液的电导率略降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
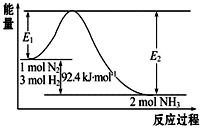 合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=Q kJ?mol-1,能量变化如图所示,回答下列问题:
合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=Q kJ?mol-1,能量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B、在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C、在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
D、某基态原子错误的核外电子排布图为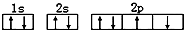 该排布图违背了泡利原理 该排布图违背了泡利原理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com