
【题目】燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。如图为氢氧燃料电池构造示意图。下列说法中正确的是( )

A.a极为电池的正极,电极反应式为:O2+4e-+2H2O=4OH-
B.b极为电池的负极,电极反应式为:H2-2e-=2H+
C.电解质溶液中K+离子向a极移动
D.当生成1molH2O时,电路中流过电子的物质的量为2mol
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 0.1mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
B. Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
C. 在Na2S溶液中加入AgC1固体,溶液中c(S2-)下降
D. pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,Ka(CH3COOH)=1.69×10-5)。
(1)醋酸钠溶液呈碱性的原因是___(写出有关的离子方程式);
(2)在CH3COONa溶液中离子浓度由大到小的顺序为___(用c(Bn+)表示相应离子浓度);
(3)对于醋酸溶液和醋酸钠溶液的下列说法正确的是___;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离
(4)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是___;
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(5)常温时,有以下3种溶液,其中pH最小的是___;
A.0.02molL1CH3COOH与0.02molL1NaOH溶液等体积混合液
B.0.01molL1CH3COOH与0.03molL1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(6)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)__pH(Na2CO3)。(填:“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①20 mL 0.01 mol/L KCl溶液 ②30 mL 0.02 mol/L CaCl2溶液
③40 mL 0.03 mol/L HCl溶液 ④10 mL 蒸馏水⑤50 mL 0.05 mol/L AgNO3溶液
A. ①>②>③>④>⑤ B. ④>①>③>②>⑤
C. ⑤>④>②>①>③ D. ④>③>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:

模拟海水中的离子浓度/mol·L-1 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol·L-1,可认为该离子不存在;实验过程中,假设溶液体积不变。Ksp[CaCO3]=4.96×10-9,Ksp[MgCO3]=6.82×10-6,Ksp[Ca(OH)2]=4.68×10-6,Ksp[Mg(OH)2]=5.61×10-12。下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液分别滴定20. 00 mL 0.1000 mol/L 盐酸和20. 00 mL 0.1000 mol/L 醋酸溶液,得到2条滴定曲线,如下图所示。
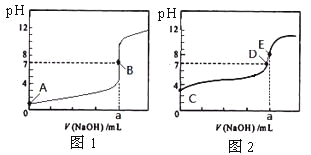
若以HA表示酸,下列说法正确的是
A. 滴定盐酸的曲线是图2
B. 达到B、D状态时,两溶液中离子浓度均为c(Na+)=C(A-)
C. 达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D. 当0 mL<V(NaOH) <20. 00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A—) >c(Na+)>c(H+) >c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是![]()
A.同时含有分子和离子的电解质溶液,一定是弱电解质溶液
B.pH为1的盐酸中,其![]() 是pH为3的盐酸中的100倍
是pH为3的盐酸中的100倍
C.室温时,![]() 的硫酸和
的硫酸和![]() 的NaOH溶液等体积混合,混合溶液的
的NaOH溶液等体积混合,混合溶液的![]()
D.![]() 溶液和
溶液和![]() 盐酸中,其水电离出的
盐酸中,其水电离出的![]() 相等
相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。试回答下列问题:
(1)Ni2+电子排布中,电子填充的能量最高的能级符号为______。
(2)金属Ni能与CO形成配合物Ni(CO)4.与CO互为等电子体的一种分子为______(写化学式,下同),与CO互为等电子体的一种离子为______。
(3)丁二酮肟(![]() )是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为______,2mol丁二酮肟分子中所含σ键的数目为______。
)是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为______,2mol丁二酮肟分子中所含σ键的数目为______。
(4)丁二酮肟常与NI2+形成图A所示的配合物,图B是硫代氧的结果:
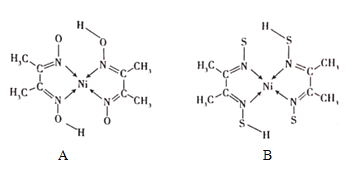
①A的熔、沸点高于B的原因为______。
②B晶体含有化学键的类型为______(填选项字母)。
A.σ键B.金属键C.配位键D.π键
(5)人工合成的氧化镍往往存在缺陷,某缺陷氧化银的组成为Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为______。
(6)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为______。
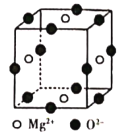
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,关于下列溶液的说法错误的是
A.某物质的溶液中由水电离出的c(H+)=1×10-10mol/L,则该溶液的pH可能为4或10
B.已知0.1 mol/L NaClO溶液的pH为9.7,0.1 mol/LNaF溶液的pH为7.5,则等体积两溶液中离子总数大小关系为:N(NaClO)>N(NaF)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/LNaOH溶液等体积混合后溶液pH大于7,则所得溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-)
D.向饱和氯水中加入NaOH溶液至PH=7,则所得溶液中:c(Na+) >c(Cl-) >c(ClO-) >c(OH-)= c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com