
【题目】下列物质中属于电解质的是( )
A. 铁 B. 熔融的氯化钠 C. 盐酸 D. SO2
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】C、N、S对应的化合物,是重要的化学物质。试回答下列问题:
(1)已知:氢气的燃烧热为286.0kJ/mol,氨气的燃烧热为382.5 kJ/mol ,则合成氨反应的热化学方程式
为_____________________。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为________________。
(3)用活性炭还原法处理氮氧化物。 有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T)条件下反应,反应进行到不同时间测得各物质的浓度如表:
时间(min) 浓度(molL-1) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为_________________。
②根据表中数据,计算T℃时该反应的平衡常数为Kp=___________,(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留两位小数)
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_________(填“增大”“不变”或“减小”)。
④该反应达到平衡时下列说法正确的是______填序号字母)。
a.容器内压强保持不变 b.2v(NO)=v(N2)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
⑤30min时改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是______。请在图中画出30~40min的变化曲线______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置:
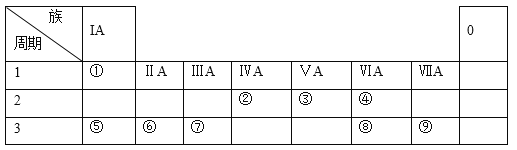
回答下列问题:
(1)写出②,③,④的气态氢化物的稳定性强弱_______________________;
(2)⑤-⑨的简单离子半径由大到小的顺序为:_______________________;(填离子符号)
(3)用电子式表示②的最高价氧化物的形成过程:____________;
(4)请设计实验比较元素⑥与⑦金属性的相对强弱:_________________;
(5) X、Y由①②④中的两种或三种元素组成。X的溶液能与小苏打反应产生Y,若X是其所属系列中最简单的分子,且相对分子质量为46,则X的名称为_________,写出X溶液与小苏打反应的离子方程式为___________________。
(6)用由①、②两种元素组成的空间构型为正四面体结构的有机物A与④元素的单质可以制成电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入A,乙极通入④的单质,则甲极的电极反应式为:_________________________________,一段时间后KOH的浓度将___(填“变大”、“变小”、“不变”或“无法确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种短周期主族元素,原子序数依次增大,X元素的气态氢化物水溶液呈碱性;Y、M同主族,可形成MY2、MY3两种分;元素Z和G可形成1:1的离子化合物,请回答下列问题:
(1)Y在元素周期表中的位置为___________.
(2)元素Y和Z按原子个数1:1形成的化合物中存在化学键的类型_____________.
(3)能说明元素G的非金属性比元素M的非金属性强的是_________(填序号).
①最高价氧化物对应水化物的酸性:G比M强
②气态氢化物的还原性:M比G强
③气态氢化物溶于水后的酸性:G比M强
④G的最高正价比M的最高正价高
(4)M和X可形成一种化合物,其相对分子质量在170~190之间,且M的质量分数约为70%,该化合物的化学式为___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向下列各个反应后所得产物的溶液中加入硫氰化钾试液,不会出现红色的是
A. Fe+Cl2(过量) → B. 稀HNO3(过量)+Fe →
C. Fe+稀硫酸(过量) → D. FeBr2(过量)+Cl2→
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
①阳离子都是由金属原子失去电子而形成的 ②非金属原子也能形成阳离子
③合金属阳离子的晶体一定是离子晶体 ④阳离子都是稳定结构,不会再失去电子
A. ①②④ B. ②③④ C. ①③④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能用勒夏特列原理解释的是
A. 使用铁触媒,加快合成氨反应速率
B. 乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利
C. 打开汽水瓶盖,即有大量气泡逸出
D. 配置FeCl3溶液时,加入少量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是
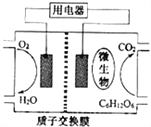
A. 该电池能够在高温下工作
B. 放电过程中,质子(H+)从正极区向负极区迁移
C. 电池的负极反应为:C6H12O6+6H2O-24e-=6CO2+24H+
D. 在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2014全国大纲卷】
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸的产率是 。
(4)用CuCl2 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com