
| 0.01mol |
| 30×10-3L |
| 1 |
| 3 |
| 0.01mol |
| 30×10-3L |
| 1 |
| 3 |
| Ksp |
| c(A2-) |
| 1.8×10-10 | ||
|


科目:高中化学 来源: 题型:
| ||
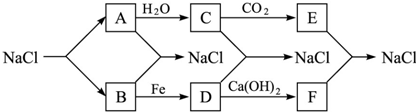
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)用工业酒精制造的假酒中通常含有
(1)用工业酒精制造的假酒中通常含有查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
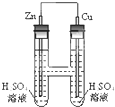 如图所示,下列叙述正确的是( )
如图所示,下列叙述正确的是( )| A、过程中溶液的PH会减小 |
| B、锌为正极,发生氧化反应 |
| C、铜棒上反应为2H++2e=H2↑ |
| D、电流方向从Zn经导线到Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钾钠合金--快中子反应堆热交换剂 |
| B、硫酸钡--钡餐、白色颜料等 |
| C、二氧化硅--光导纤维、半导体材料 |
| D、硫酸铜--净水、治疗鱼类皮肤病 |
查看答案和解析>>
科目:高中化学 来源: 题型:
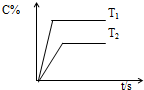 对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )
对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )| A、T1>T2,△H>0 |
| B、T1>T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1<T2,△H<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com