
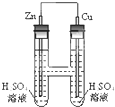
 如图所示,下列叙述正确的是( )
如图所示,下列叙述正确的是( )| A、过程中溶液的PH会减小 |
| B、锌为正极,发生氧化反应 |
| C、铜棒上反应为2H++2e=H2↑ |
| D、电流方向从Zn经导线到Cu |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg+2H+=Mg2++H2↑ | ||||
B、C+CO2
| ||||
C、H2+Cl2
| ||||
D、2Al+Fe2O3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用添加瘦肉精的饲料喂猪 |
| B、用福尔马林保鲜水产品 |
| C、用二氧化硫气体漂白竹笋 |
| D、用小苏打做发酵粉做糕点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向碳酸氢钠溶液滴加NaOH溶液 HCO3-+OH-=CO32-+H2O |
| B、MgO溶于盐酸中:O2-+2H+=H2O |
| C、镁和稀硫酸反应 Mg+2H+=Mg2++H2↑ |
| D、氯气与水反应 Cl2+H2O?2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与电源负极相连的铁丝圈叫阴极 |
| B、与电源正极相连的石墨棒叫阳极 |
| C、随着电解的进行,阳极附近溶液的pH显著升高 |
| D、阳极放出的气体能使湿润的淀粉碘化钾试纸变蓝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com