
����Ŀ����ͼ����Ӧ��Ϊ�����µķ�Ӧ��A��C��D�о�������Ԫ�أ���A����Ԫ�صĻ��ϼ۽���C��D����Ԫ�صĻ��ϼ�֮�䣬E�ڳ�����Ϊ��ɫ��ζ��Һ�壬F�ǵ���ɫ���壬GΪ��������ɫ���塣��ش��������⣺
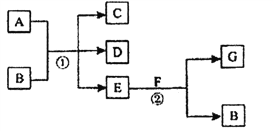
��1��A��G�Ļ�ѧʽ�ֱ�Ϊ_______________��________________��
��2��д��A��Fe��Ӧ�Ļ�ѧ����ʽ___________________ ��
��3��д����Ӧ�ڵĻ�ѧ����ʽ______________________��
��4����֪A��һ����Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ������������������Ҫ��Ӧ�á��������ѧ֪ʶ�ش��������⡣
�ٽ�Aͨ����ɫʯ����Һ�У��۲쵽��������________________����д��A��ˮ��Ӧ�Ļ�ѧ����
ʽ ��
��A��ʯ���鷴Ӧ�Ƶõ�Ư�۵���Ч�ɷ���_________(�ѧʽ)���������ڿ�����ʧЧ��ԭ��______(�û�ѧ����ʽ��ʾ)��
���𰸡� Cl2��O2 2Fe+3Cl2=2FeCl3 (��ȼ�� 2Na2O2+2H2O=4NaOH+O2�� �ȱ�����ɫ Cl2+H2O=HCl+HClO Ca(C1O)2 Ca(ClO)2+CO2+H2O=CaCO3��+2HClO��2HClO=2HCl+O2��(��)
�����������������E������Ϊ��ɫ��ζ��Һ�壬ӦΪH2O��FΪ����ɫ��ĩ��ӦΪNa2O2����GΪO2��BΪNaOH��A��C��D������Ԫ�أ���A����Ԫ�صĻ��ϼ۽���C��D֮�䣬ӦΪCl2��NaOH�ķ�Ӧ������NaCl��NaClO��
(1)�����Ϸ�����֪AΪCl2��GΪO2���ʴ�Ϊ��Cl2�� O2��
(2)Fe��������ȼ�յĻ�ѧ����ʽΪ2Fe + 3Cl2![]() 2FeCl3���ʴ�Ϊ��2Fe + 3Cl2
2FeCl3���ʴ�Ϊ��2Fe + 3Cl2![]() 2FeCl3��
2FeCl3��
(3)��Ӧ���ǹ���������ˮ�ķ�Ӧ����ѧ����ʽΪ2Na2O2+2H2O=4 NaOH +O2�����ʴ�Ϊ��2Na2O2+2H2O=4 NaOH +O2����
(4)��������ͨ����ɫʯ����Һ�У��۲쵽����������ɫ��Һ�ȱ�����ɫ��������ˮ��Ӧ�Ļ�ѧ����ʽΪCl2+H2O![]() HCl+HClO���ʴ�Ϊ����ɫ��Һ�ȱ�����ɫ��Cl2+H2O
HCl+HClO���ʴ�Ϊ����ɫ��Һ�ȱ�����ɫ��Cl2+H2O![]() HCl+HClO��
HCl+HClO��
��������ʯ���鷴Ӧ�Ƶõ�Ư�۵���Ч�ɷ���Ca(ClO)2���������ڿ������ܹ��������̼��ˮ������ӦʧЧ����ѧ����ʽΪCa(ClO)2+CO2+H2O=CaCO3��+2HclO��2HClO![]() 2HCl+ O2�����ʴ�Ϊ��Ca(ClO)2��Ca(ClO)2+CO2+H2O=CaCO3��+2HclO��2HClO
2HCl+ O2�����ʴ�Ϊ��Ca(ClO)2��Ca(ClO)2+CO2+H2O=CaCO3��+2HclO��2HClO![]() 2HCl+ O2����
2HCl+ O2����


 ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д� ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ʳƷ���Ӽ�������������ǣ� ��
A. ����������һ���°����� B. Ӫ��ǿ����Ҳ��һ��ʳƷ���Ӽ�
C. ��ͬʱ������ζ���ͷ����� D. ���ܲ��غ����ʻ��dz�������ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ڹ�ũҵ����������Ӧ�ù㷺�������������⡣
��1������ͭ��Һʱ���������ж���һ�ֽⶾ����
P4+CuSO4+H2O![]() Cu3P+H3PO4+H2SO4����6molH3PO4��������CuSO4������P4�����ʵ���Ϊ ��
Cu3P+H3PO4+H2SO4����6molH3PO4��������CuSO4������P4�����ʵ���Ϊ ��
��2�����Ļ�����ϳɡ�Ӧ�ü����Ĺ̶�һֱ�ǿ�ѧ�о����ȵ㡣��CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3(g����CO2(g����NH2CO2NH4(s������H����159.47 kJ��mol��1
��NH2CO2NH4(s����CO (NH2��2(s����H2O(g������H��a kJ��mol��1
��2NH3(g����CO2(g����CO(NH2��2(s����H2O(g������H����86.98 kJ��mol��1
��aΪ ��
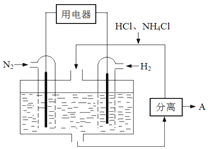
��3����ͼ��ʾʹ�����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ����������ṩ������ͬʱ����ʵ�ֵ��̶�������ȼ�ϵ�ء���д���õ�ص�������Ӧʽ �������пɷ����������A�Ļ�ѧʽΪ ��
��4������������0.1mol/L��ˮ�м�������N2O5��ʹ��Һ��c(NH3��H2O��:c(NH4+��=5��9,��ʱ��Һ��pH= .(25��ʱ��NH3��H2O�ĵ��볣��Kb=1.8��10-5��
��5��SiO2��������������һ�ּ�ǿ�Ķ�Ԫ���ˮ��������������3��Ԫ����ɣ����з�Ԫ������������Ϊ79.17%����д��SiO2�������������ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڹ��ȷ����ߵ������У��������������� �� ��
A. ˮ B. ֬�� C. ������ D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ã�����Һa�������b��, ���������в���ȷ���ǣ� ��
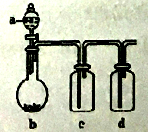
A����aΪŨ���ᣬbΪNa2SO3���壬c��ʢʯ����Һ����c����Һ�ȱ�����ɫ
B����aΪŨ���ᣬbΪMnO2��c��ʢƷ����Һ����c����Һ����ɫ
C����aΪ������Һ��bΪ���ǣ�c��ʢ��������ʯ��ˮ����c����Һ�����
D����aΪŨ��ˮ��bΪ��ʯ�ң�c��ʢAlCl3��Һ����c�в�����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������أ������й�˵��������ǣ� ��
A�������յķ����������ֲ�˿��������ά
B��ʳ���ͷ������Ȼ�����������������к�����
C��������ɱ�����в�������Ϊ���������ȱ���
D��ҽ�������ƾ����Ҵ���Ũ��Ϊ95%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⻯��(NaBH4��Ϊ��ɫ��ĩ��������ˮ���⣬�����������(�۵㣺-101�����е㣺33�������ڸɿ������ȶ�����ʪ�����зֽ⣬�����ϳɺ��л��ϳ��г��õ�ѡ���Ի�ԭ����ij�о�С�����ƫ������(NaBO2��Ϊ��Ҫԭ���Ʊ�NaBH4�����������£�����˵������ȷ����( ��
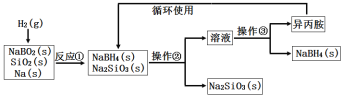
A��ʵ������ȡ����������Ҫ�õ���ʵ����Ʒ�����ӡ���ֽ������Ƭ��С��
B�����������������ֱ��ǹ����������ᾧ
C����Ӧ������֮ǰ�轫��Ӧ��������100�����ϲ�ͨ�����
D����Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
A. Fe��Mn��Zn��Mg
B. Zn��Cu��Mn��Ca
C. Zn��Cu��B��Mn
D. Mg��Mn��Cu��Mo
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2+3H2![]() 2NH3�տ�ʼʱ��N2��Ũ��Ϊ3mol/L��H2��Ũ��5mol/L��3min����NH3Ũ��Ϊ0.6mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����( )
2NH3�տ�ʼʱ��N2��Ũ��Ϊ3mol/L��H2��Ũ��5mol/L��3min����NH3Ũ��Ϊ0.6mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����( )
A��v(NH3)=0.2mol/(L��min) B��v(N2)=1mol/(L��min)
C��v(H2)=1.67mol/(L��min) D��v(H2)=1.37mol/(L��min)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com