
【题目】下列关于海水资源的说法不正确的是( )
A. 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B. 从海水中可以提取铀和重水等核原料
C. 海水中的溴、氟等元素均为微量元素,但仍有提取的价值
D. 海水中金的储存量约为陆地的170倍,但它的富集程度却很低
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】在200mL MgCl2、AlCl3的混合溶液中,c(Mg2+)=0.2mol/L、c(Cl)=1.3mol/L,若要使其中的Mg2+全部转化为沉淀而分离出来,至少需要4mol/L的NaOH溶液的体积为( )
A.120mL B.80mL C.40mL D.20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。

已知:①反应![]() 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和![]() 可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
(1)①中反应的化学方程式为_____________________;
(2)化合物Ⅰ的电子式为________________,它的空间构型是_________;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,至少所需铜粉的质量为 g;
(4)C与过量NaOH溶液反应的离子方程式为_____________,反应后溶液与过量化合物Ⅰ反应的离子方程式:__________________;
(5)实验室中一般检验I存在的试剂和方法是:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷的叙述正确的是( )
A.天然气的主要成分甲烷燃烧时放出大量热量,属于重要的二次能源
B.甲烷分子中四个碳氢单键的性质完全相同,分子结构为平面正方形
C.甲烷和氯气反应生成的二氯甲烷没有同分异构现象
D.甲烷的化学性质比较稳定,不被任何氧化剂氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度 T 时水的离子积常数为 Kw,该温度下,将浓度为 amol/L 的一元酸HA 与 bmol/L 的一元碱 BOH 等体积混合,可判断该溶液呈中性的依据是:
A.a=b
B.混合溶液的 pH 值为 7
C.混合溶液中C(H+)=![]()
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在烷烃分子中的基团:CH3、CH2、![]() 、
、![]() 中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用nl、n2、n3、n4表示。
中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用nl、n2、n3、n4表示。
例如: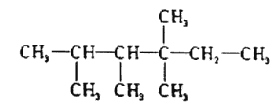 分子中,nl=6,n2=1,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
分子中,nl=6,n2=1,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子数为A,A与nl、n2、n3、n4的关系是:A=_________,或A=_________。
(2)四种碳原子数之间的关系为nl=____________。
(3)若某分子中n2=n3=n4=1,写出该分子的结构简式和键线式,并对其进行命名:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产联系密切,下列说法不正确的是( )
A.生石灰、铁粉常用于食品干燥剂
B.“地沟油”经过加工处理后可用来制肥皂
C.抗酸药如小苏打可治疗因胃酸过多引起的消化不良
D.以粮食为原料酿酒过程的变化包括粮食→淀粉→葡萄糖→乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1 L的密闭容器中,发生如下反应:CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )
A.该反应的ΔH>0、T1<T2
B.T2时CH4的平衡转化率为30.0%
C.T2时40min后,断裂4mol C-H键同时断裂4 mol O-H键
D.T1时向平衡体系中再充入CH4,建立平衡后CO2的体积分数一定增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com