


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,下列说法错误的是( )
2SO3,下列说法错误的是( )| A.增大氧气的浓度可提高反应速率 |
| B.升高温度可提高反应速率 |
| C.使用催化剂能显著增大反应速率 |
| D.达到化学平衡时正逆反应速率相等且都为零 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定条件下,增大反应物的量会加快化学反应速率 |
| B.增大压强,肯定会加快化学反应速率 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.能够发生有效碰撞的分子叫活化分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与水反应时,增加水的量 |
| B.锌与稀硫酸反应时,加入少量CuSO4固体 |
| C.用18mol/L的硫酸溶液代替 2mol/L硫酸溶液常温下与铝反应 |
| D.合成氨反应,恒容通入氦气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入蒸馏水 | B.加热 | C.加入NaCl溶液 | D.加入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
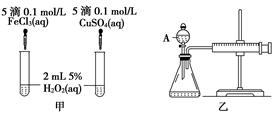
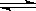 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________ | A.容器内的压强不随时间而变化 |
| B.混合气的密度不再随时间而变化 |
| C.A的质量不再改变 |
| D.平衡混合气体的平均相对分子质量不再改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com