
【题目】已知在25 ℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为
醋酸 K=1.75×10-5 次氯酸 K=2.95×10-8
碳酸 K1=4.0×10-7 K2=5.0×10-11
亚硫酸 K1=1.54×10-2 K2=1.02×10-7
(1)常温下,写出碳酸的第一级电离平衡常数表达式K1=__________,则0.50mol/L的Na2CO3溶液的pH=________
(2)等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小顺序为_____________。
(3)向0.01molL-1CH3COONa溶液中分别加入少量浓盐酸、Na2CO3固体使水解平衡移动的方向分别为___________、________.(填“左”“右”或“不移动”)
(4)物质的量浓度均为0.1 mol/L的CH3COONa和CH3COOH溶液等体积混合混合液中的下列关系式正确的是________。
A.c(CH3COOH)+2c(OH-)=c(CH3COO-)+2c(H+)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.2mol/L
D. c(CH3COOH) > c(Na+) > c(CH3COO-) > c(H+) > c(OH-)
(5)下列离子方程式中错误的是________。
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-===HCO![]() +HClO
+HClO
B.少量SO2通入次氯酸钙溶液中:2ClO-+SO2+H2O===SO32-+2HClO
C.Na2CO3溶液中加入足量NaHSO3溶液: CO32-+HSO3-=HCO3-+SO32-
D.少量CO2通入亚硫酸钠溶液中: SO32-+CO2+H2O=HSO3-+HCO3-
【答案】 ![]() 12 c(Na+)>c(HCO
12 c(Na+)>c(HCO![]() )>c(CO
)>c(CO![]() )>c(OH-)>c(H+) 右 左 B B
)>c(OH-)>c(H+) 右 左 B B
【解析】(1)根据电离平衡常数的含义可得碳酸的第一级电离平衡常数表达式K1=![]() ;根据反应CO32-+H2O
;根据反应CO32-+H2O![]() HCO3-+OH-,则Kh=
HCO3-+OH-,则Kh=![]() ,0.50mol/L的Na2CO3溶液按一元弱碱计算:c(OH-)=
,0.50mol/L的Na2CO3溶液按一元弱碱计算:c(OH-)=![]() =
=![]() ,pH=12;(2)等浓度的Na2CO3和NaHCO3的混合溶液,由于HCO3—、CO32—都会发生水解反应,而且水解程度HCO3—< CO32—,水解是溶液显碱性,c(OH-)>c(H+);但是盐水解的程度是微弱的,主要还是以盐电离产生的离子存在,所以根据物料守恒可得c(Na+)>c(HCO3—)>c(CO32—)。故溶液中各离子浓度大小顺序为c(Na+)>c(HCO3—)>c(CO32—)>c(OH-)>c(H+);(3)向0.01mol/LCH3COONa溶液中存在水解平衡,CH3COO-+H2O
,pH=12;(2)等浓度的Na2CO3和NaHCO3的混合溶液,由于HCO3—、CO32—都会发生水解反应,而且水解程度HCO3—< CO32—,水解是溶液显碱性,c(OH-)>c(H+);但是盐水解的程度是微弱的,主要还是以盐电离产生的离子存在,所以根据物料守恒可得c(Na+)>c(HCO3—)>c(CO32—)。故溶液中各离子浓度大小顺序为c(Na+)>c(HCO3—)>c(CO32—)>c(OH-)>c(H+);(3)向0.01mol/LCH3COONa溶液中存在水解平衡,CH3COO-+H2O![]() CH3COOH+OH-使溶液显碱性;加入少量浓盐酸平衡右移、加入Na2CO3固体溶解后碳酸根离子水解显碱性使水解平衡左移;(4)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为①c(Na+)+c(H+)=c(CH3COO-)+c(OH-),选项B正确;物料守恒为②c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),选项C错误;①×2,然后②式代入得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),选项A错误;醋酸根离子水解,溶液显碱性,显性离子大于隐性离子,则离子关系为
CH3COOH+OH-使溶液显碱性;加入少量浓盐酸平衡右移、加入Na2CO3固体溶解后碳酸根离子水解显碱性使水解平衡左移;(4)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为①c(Na+)+c(H+)=c(CH3COO-)+c(OH-),选项B正确;物料守恒为②c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),选项C错误;①×2,然后②式代入得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),选项A错误;醋酸根离子水解,溶液显碱性,显性离子大于隐性离子,则离子关系为
c(Na+) > c(CH3COO-) > c(OH-)> c(H+),选项D错误。答案选B;(5)A、由于酸性H2CO3>HClO> HCO3— ,所以少量CO2通入次氯酸钠溶液中,会发生反应:CO2+H2O+ClO-===HCO![]() +HClO,正确;B.由于HClO有强氧化性,而H2SO3有还原性,所以少量SO2通入次氯酸钙溶液中,会发生氧化还原反应:Ca2++ClO-+SO2+H2O===CaSO4↓+2H++Cl-,错误;C.Na2CO3溶液中加入足量NaHSO3溶液: CO32-+HSO3-=HCO3-+SO32-,正确;D、少量CO2通入亚硫酸钠溶液中: SO32-+CO2+H2O=HSO3-+HCO3-,正确。答案选B。
+HClO,正确;B.由于HClO有强氧化性,而H2SO3有还原性,所以少量SO2通入次氯酸钙溶液中,会发生氧化还原反应:Ca2++ClO-+SO2+H2O===CaSO4↓+2H++Cl-,错误;C.Na2CO3溶液中加入足量NaHSO3溶液: CO32-+HSO3-=HCO3-+SO32-,正确;D、少量CO2通入亚硫酸钠溶液中: SO32-+CO2+H2O=HSO3-+HCO3-,正确。答案选B。


科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述正确的是

A. a和b不连接时,铁片上会发生氧化反应而质量减少
B. a和b用导线连接时,铜片上发生的反应为:Cu-2e-===Cu2+
C. 无论a和b是否连接,铁片均会被氧化,溶液均有Fe2+生成
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)B中发生反应的离子方程式为_______________________________________________。
(2)为了获得纯净干燥的氯气,D中应放入的试剂为_______。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是__________________________。
(4)G是浸有淀粉KI溶液的棉花球,G 处现象是棉花球表面变成________________。
(5)整套装置存在不妥之处,原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境日益引起人们的重视。下列做法有利于保护环境的是( )
A. 氢能源代替化石能源
B. 推广使用太阳能电池
C. 电动汽车代替燃油汽车
D. 造纸厂污水直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是25℃时几种难溶电解质的溶度极数值:
难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 1.0×10-12 | 1.0×10-20 | 1.0×10-16 | 1.0×10-38 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为___________(填名称)而除去。
(2)①中加入的试剂应选择________为宜,其原因是_______________________________。
(3)②中除去Fe3+所发生的总反应的离子方程式__________________________________。
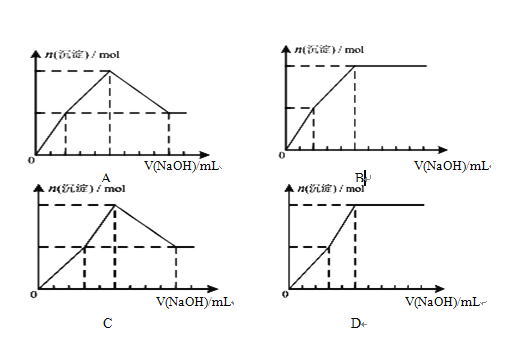
(4) 向浓度均为0.1mol/L-1的Fe(NO3)3和Cu(NO3)2混合溶液中,逐滴加入NaOH.下列示意图表示生成沉淀的总物质的量与加入NaOH的体积的关系,合理的是(____)
(5)若将某MgCl2、FeCl3均为0.1 mol·L-1混合溶液中的pH用MgO调整至pH=4,则溶液中![]() 比值约为______________________。
比值约为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装有 Fe2O3、 CuO、 Fe、 Cu 的烧杯中加入过量稀硫酸,充分反应后,仍有红色粉末剩余,则关于反应后溶液中金属阳离子的判断一定正确的是
A. 一定有Fe2+,可能有Cu2+ B. 只有Fe2+
C. 一定有Fe2+、Cu2+,可能有Fe3+ D. 只有Fe2+和Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子,如N3-、N3-、NH2-、NH4+、N2H5+、N2H62+ 等,已知H2O结合一个H+可得到H3O+,N2H5+与N2H62+是由中性分子X结合H+形成的,有类似于NH4+的性质。
⑴ 形成N2H5+离子的中性分子X的结构式是______________;
⑵ X在氧气中可以燃烧,写出燃烧反应的化学方程式_______________________________;
⑶ 写出N2H62+离子在足量强碱溶液中反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有下列离子中的若干种:K+、Na+、Fe2+、Fe3+、SO![]() 、I-、CO
、I-、CO![]() ,现取三份20 mL该溶液进行如下实验:
,现取三份20 mL该溶液进行如下实验:
①第一份加入足量盐酸,无任何气体产生
②第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧,最后得到x g固体
③第三份滴加0.10 mol·L-1酸性KMnO4溶液,恰好完全反应,消耗其体积为V mL
④另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色
根据上述实验,以下说法正确的是
A. 由实验②、③可判定原混合溶液中是否存在I-
B. 由实验①可推断原混合溶液中是否含有SO![]()
C. 由实验③可判定原混合溶液中是否含有Fe2+
D. 原混合溶液中只存在Na+、Fe3+、SO![]() ,不可能存在K+、CO
,不可能存在K+、CO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com