
【题目】下列说法正确的是
A.晶体硅常用于制作光导纤维
B.钠能从溶液中置换出金属活动顺序表中钠后面的金属
C.蒸馏时,冷凝水从冷凝管上管口进,由下管口出
D.碘水中萃取碘时,往分液漏斗中先后加入碘水和四氯化碳,充分振荡静置后分液
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】有机化合物甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO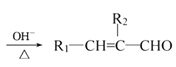 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的分子式是____,G中含氧官能团的名称是____。
(2)②的反应类型是____, F的结构简式为______。
(3)B的核磁共振氢谱有____组峰,峰面积之比为_____________。
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式:_____________。
(6)设计实验检验E中的官能团(说明实验操作步骤、现象及结论)____________
(7)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置制备并检验Cl2的性质,下列说法正确的是
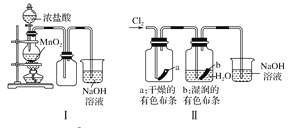
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B. Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气
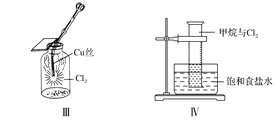
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:量筒中发生了加成反应,量筒内液面上升,量筒壁上有无色液滴出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个装有CH4和Cl2 混合气体的集气瓶,用玻璃片盖好瓶口后,分别作如下处理,各有怎样的现象发生?
(1)①置于黑暗中: _____________________;
②将点燃的镁条靠近集气瓶外壁: ________________________;
③放在有光线的房子里: __________________________________。
(2)CH4和Cl2发生的一系列反应都是___________(填反应类型)反应,请写出CH4和Cl2反应生成一氯甲烷的化学方程式: ________________________________。
(3)若要使0.5 mol CH4完全和Cl2发生取代反应,并生成相同物质的量的四种取代产物,则生成HCl的物质的量为_________。
A.2.5mol B.2mol C.1.25mol D.0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容密闭容器中发生反应2A(g)+B(g)![]() 2C(g),若反应物A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.036 mol·L-1所需的时间为( )
2C(g),若反应物A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.036 mol·L-1所需的时间为( )
A. 等于10 s B. 等于12 s
C. 大于12 s D. 小于12 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,配制一组c(H2A)+ c(HA-)+ c(A2-)=0.100 mol·L-1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法正确的是

A. H2A在水中的电离方程式为:H2A=HA-+ H+,HA-![]() H++A2-
H++A2-
B. c(Na+)=0.100 mol·L-1的溶液中,c(H+)+c(H2A)=c(OH-)+ c(A2-)
C. pH=4的溶液中,c(HA-)>c(H2A)+ c(A2-)
D. pH=7的溶液中,c(Na+)=2c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从工业含锌废渣(主要成分为ZnO,还含有SiO2、Fe3+、Cu2+、Pb2+等杂质)制取ZnCO32Zn(OH)2的一种工艺如下:
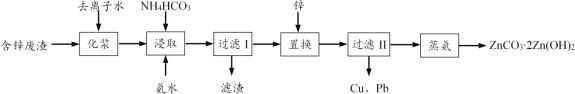
(1)浸取前,需将含锌废渣粉碎并加水制成悬浊液(化浆),目的是____。
(2)浸取时的温度控制在30 ℃,原因是____。浸取后,ZnO转化为[Zn(NH3)4]CO3溶液,滤渣的主要成分为____。
(3)除Cu2+、Pb2+时,也可加入(NH4)2S使其生成硫化物沉淀。已知Ksp(CuS)=6.310-36,Ksp(PbS)=8.010-28,要使溶液中Cu2+、Pb2+的浓度均小于1.010-5 mol·L-1,则沉淀时需控制S2-的浓度至少为_____mol·L-1。
(4)蒸氨时发生反应的化学方程式为____。
(5)本工艺中可循环利用的物质为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化。在100 mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50.0 | 120.0 | 232.0 | 290.0 | 312.4 |
(1)解释2 min~3 min反应速率最大的原因______;反应速率最小的时间段是_____,原因为____。
(2)在4min~5 min时间段内,用盐酸的浓度变化表示的反应速率为____。
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A. Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4 (s)![]() 2NH3 (g)+ CO2 (g) 。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3 (g)+ CO2 (g) 。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
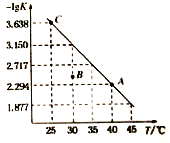
A. C点对应状态的平衡常数K(C)=10-3.638
B. 该反应的△H>0
C. NH3的体积分数不变时,该反应一定达到平衡状态
D. 30 ℃时,B点对应状态的v(正)<v(逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com