
【题目】有机化合物甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO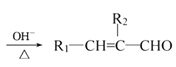 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的分子式是____,G中含氧官能团的名称是____。
(2)②的反应类型是____, F的结构简式为______。
(3)B的核磁共振氢谱有____组峰,峰面积之比为_____________。
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式:_____________。
(6)设计实验检验E中的官能团(说明实验操作步骤、现象及结论)____________
(7)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
【答案】 C7H8 羧基 加成反应 ![]() 4组峰 2:2:2:1 4
4组峰 2:2:2:1 4 ![]() +CH3COOH
+CH3COOH![]()
![]() +H2O 取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键
+H2O 取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键 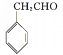
![]()
![]()
![]()
![]()
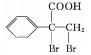
【解析】D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39,则相对分子质量为78,结合Cl3CCHO与D反应生成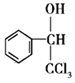 可推出D为苯,A为苯的同系物,且经过多步反应生成苯甲醛,故A为甲苯,甲苯在光照条件下与氯气发生取代反应生成B为
可推出D为苯,A为苯的同系物,且经过多步反应生成苯甲醛,故A为甲苯,甲苯在光照条件下与氯气发生取代反应生成B为![]() ,
,![]() 在氢氧化钠的水溶液中加热发生取代反应生成C为
在氢氧化钠的水溶液中加热发生取代反应生成C为![]() ,
,![]() 在铜的催化下发生氧化反应生成
在铜的催化下发生氧化反应生成![]() ,
,![]() 与乙醛在稀氢氧化钠溶液中加热发生加成反应得到E为
与乙醛在稀氢氧化钠溶液中加热发生加成反应得到E为![]() ,
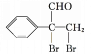
,![]() 与溴的四氯化碳溶液发生加成反应生成F为
与溴的四氯化碳溶液发生加成反应生成F为![]() ,
,![]() 在催化剂作用下与氧气发生氧化反应生成G为
在催化剂作用下与氧气发生氧化反应生成G为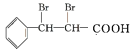 。(1)A为甲苯,分子式是C7H8,G为
。(1)A为甲苯,分子式是C7H8,G为 ,含氧官能团的名称是羧基;(2)②是
,含氧官能团的名称是羧基;(2)②是![]() 与三氯甲烷在碱溶液中发生加成反应生成
与三氯甲烷在碱溶液中发生加成反应生成 ,反应类型是加成反应, F的结构简式为
,反应类型是加成反应, F的结构简式为![]() ;(3)B为
;(3)B为![]() ,的核磁共振氢谱有4组峰,峰面积之比为2:2:2:1;(4)C为
,的核磁共振氢谱有4组峰,峰面积之比为2:2:2:1;(4)C为![]() ,有多种同分异构体,其中属于芳香族化合物的有甲苯醚、对甲基苯酚、间甲基苯酚、邻甲基苯酚共4种;(5)反应①是
,有多种同分异构体,其中属于芳香族化合物的有甲苯醚、对甲基苯酚、间甲基苯酚、邻甲基苯酚共4种;(5)反应①是 与乙酸发生酯化反应生成
与乙酸发生酯化反应生成![]() ,反应的化学方程式为:
,反应的化学方程式为: ![]() +CH3COOH
+CH3COOH![]()
![]() +H2O;(6)E为
+H2O;(6)E为![]() ,所含官能团为碳碳双键和醛基,必须先检验醛基再检验碳碳双键,故检验方法为:取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键;(7)G的同分异构体
,所含官能团为碳碳双键和醛基,必须先检验醛基再检验碳碳双键,故检验方法为:取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键;(7)G的同分异构体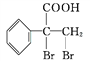 是一种重要的药物中间体,其合成路线与G相似,
是一种重要的药物中间体,其合成路线与G相似, ![]() 与甲醛在稀氢氧化钠溶液中加热反应生成
与甲醛在稀氢氧化钠溶液中加热反应生成![]() ,
,![]() 与溴的四氯化碳溶液反应生成
与溴的四氯化碳溶液反应生成 ,
, 催化氧化得到
催化氧化得到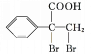 ,合成路线如下:
,合成路线如下: 
![]()
![]()
![]()

![]()

。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3===K2O+5Na2O+16N2↑下列说法正确的是:
A. KNO3是还原剂,其中氮元素被氧化
B. 生成物中的N2是氧化产物,K2O是还原产物
C. 每转移1 mol电子,可生成标准状况下N2的体积为35.84 L
D. 若有65 g NaN3参加反应,则被氧化的N的物质的量为3.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某饭店计划将燃料从煤气改为天然气,灶具应作相应调整,正确的方法是( )
A.空气和天然气进入量都减小
B.增大空气进入量或减小天然气进入量
C.空气和天然气进入量都增大
D.增大天然气进入量或减小空气进入量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 2NH4Cl(s)+ Ca(OH)2(s)![]() CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
(1)产生的氨气在标准状况时的体积为多少?
(2)将所得氨气全部溶于200mL水中,若所得氨水的密度为0.936 g·cm-3,则该氨水的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘对动植物的生命是极其重要的,海水里的碘化物和碘酸盐参与大多数海生物的新陈代谢。在高级哺乳动物中,碘以碘化氨基酸的形式集中在甲状腺内,缺乏碘会引起甲状腺肿大。
I.现要从工业含碘废液中回收碘单质(废液中含有H2O、油脂、I2、I)。设计如图一所示的实验过程:
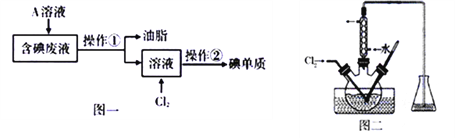
(1)为了将含碘废液中的I2完全转化为I—而进入水层,向含碘废液中加入了稍过量的A溶液,则A应该具有___________性。
(2)将在三颈烧瓶中反应完全后的溶液经过操作②获得碘单质,操作②包含多步操作,操作名称分别为萃取、_____、_____,在操作②中必须用到下列所示的部分仪器或装置,这些仪器和装置是________________(填标号)。
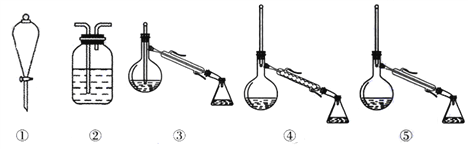
(3)将操作①所得溶液放入图二所示的三颈烧瓶中,并用盐酸调至pH约为2,再缓慢通入适量Cl2,使其在30~40℃反应。写出其中发生反应的离子方程式________________;Cl2不能过量,因为过量的Cl2将I2氧化为IO3-,写出该反应的离子方程式__________。
II.油脂的不饱和度可通过油脂与碘的加成反应测定,通常称为油脂的碘值。碘值越大,油脂的不饱和程度越高。碘值是指100g油脂所能吸收的I2的克数。称取xg某油脂,加入含ymol I2的韦氏溶液(韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用cmol/L Na2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液V mL(滴定反应为:2Na2S2O3+I2=Na2S4O6+2NaI)。回答下列问题:
(1)下列有关滴定的说法不正确的是________(填标号)。
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C. 滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是_______________________________________________。
(3)该油脂的碘值为_____g(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。

(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:
![]()
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 处于最低能量的原子叫做基态原子
B. 原子由基态变为激发态要产生发射光谱
C. 同一原子中,2p能级比3p能级的轨道数少
D. 3d轨道能量小于4s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A(g)+B(g) ![]() C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
温度/℃ | 700 | 830 | 1200 |
K值 | 1.7 | 1.0 | 0.4 |
A. 达到平衡后,B的转化率为50%
B. 增大压强,正、逆反应速率均加快
C. 该反应为吸热反应,升高温度,平衡正向移动
D. 反应初始至平衡,A的平均反应速率v(A)=0.005 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com