
【题目】碘对动植物的生命是极其重要的,海水里的碘化物和碘酸盐参与大多数海生物的新陈代谢。在高级哺乳动物中,碘以碘化氨基酸的形式集中在甲状腺内,缺乏碘会引起甲状腺肿大。
I.现要从工业含碘废液中回收碘单质(废液中含有H2O、油脂、I2、I)。设计如图一所示的实验过程:
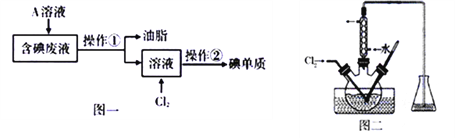
(1)为了将含碘废液中的I2完全转化为I—而进入水层,向含碘废液中加入了稍过量的A溶液,则A应该具有___________性。
(2)将在三颈烧瓶中反应完全后的溶液经过操作②获得碘单质,操作②包含多步操作,操作名称分别为萃取、_____、_____,在操作②中必须用到下列所示的部分仪器或装置,这些仪器和装置是________________(填标号)。
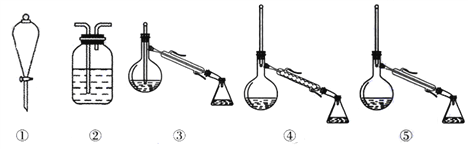
(3)将操作①所得溶液放入图二所示的三颈烧瓶中,并用盐酸调至pH约为2,再缓慢通入适量Cl2,使其在30~40℃反应。写出其中发生反应的离子方程式________________;Cl2不能过量,因为过量的Cl2将I2氧化为IO3-,写出该反应的离子方程式__________。
II.油脂的不饱和度可通过油脂与碘的加成反应测定,通常称为油脂的碘值。碘值越大,油脂的不饱和程度越高。碘值是指100g油脂所能吸收的I2的克数。称取xg某油脂,加入含ymol I2的韦氏溶液(韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用cmol/L Na2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液V mL(滴定反应为:2Na2S2O3+I2=Na2S4O6+2NaI)。回答下列问题:
(1)下列有关滴定的说法不正确的是________(填标号)。
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C. 滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是_______________________________________________。
(3)该油脂的碘值为_____g(列式表示)。
【答案】 还原性 分液 蒸馏 ①⑤ Cl2+2I—=2Cl—+I2 5Cl2+I2+6H2O=10C1-+2IO3-+12H+ BD 韦氏液中的CH3COOH消耗Na2S2O3,使滴定过程消耗的Na2S2O3偏大,导致测出的与油脂反应的I2偏少 (25400y-12.7cV)/x或[(y-1/2cV×10-3)/x]×25400或(25400y-12700cV×10-3)/x
【解析】I.(1)将含碘废液中的I2完全转化为I—而进入水层,碘由0价变为-1价被还原,故向含碘废液中加入了稍过量的A溶液,则A应该具有还原性;(2)操作②将水溶液中的碘萃取后分液得到含有碘的有机溶液,利用有机物和碘的沸点不同再进行蒸馏,故包含的操作名称分别为萃取、分液、蒸馏,在操作②中萃取、分液需要用到分液漏斗,蒸馏需要用到相应蒸馏装置,答案选①⑤; (3)Cl2将碘离子氧化生成碘单质,发生反应的离子方程式为Cl2+2I—=2Cl—+I2;Cl2不能过量,因为过量的Cl2将I2氧化为IO3-,反应的离子方程式为5Cl2+I2+6H2O=10C1-+2IO3-+12H+;II. (1)A.标准Na2S2O3溶液呈碱性,应盛装在碱式滴定管中,选项A正确;B.滴定时眼睛只要注视锥形瓶中溶液颜色的变化,选项B不正确;C. 滴定终点时,俯视读数,所读标准液体积偏小,导致测定结果偏低,选项C正确;D.滴定前锥形瓶内溶液呈蓝色,滴定到溶液由蓝色变为无色时,并且半分钟内不变色,达到滴定终点,选项D不正确。答案选BD; (2)韦氏液中的CH3COOH消耗Na2S2O3,使滴定过程消耗的Na2S2O3偏大,导致测出的与油脂反应的I2偏少;(3)根据反应2Na2S2O3+I2=Na2S4O6+2NaI,Na2S2O3溶液消耗碘的物质的量是![]() ,设某油脂碘的质量为ag,
,设某油脂碘的质量为ag,![]() ,a=254y-127cV×10-3,该油脂的碘值为
,a=254y-127cV×10-3,该油脂的碘值为![]() 。
。


科目:高中化学 来源: 题型:
【题目】一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
A. 5∶3 B. 5∶4 C. 1∶1 D. 3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
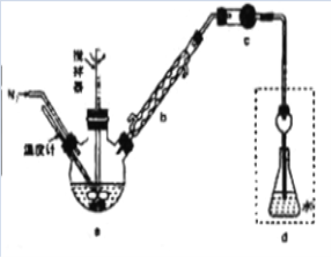
【题目】某实验兴趣小组将无水FeCl3与氯苯混合发生反应制备常用还原剂FeCl2,反应原理是:2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑。按照如图装置,在三颈烧瓶中放入162.5g无水FeCl3和225g氯苯,控制反应温度在130℃下加热3h,冷却、过滤、洗涤、干燥得到粗产品。将生成的HCl用水吸收,利用莫尔法可以测出无水FeCl3的转化率(莫尔法是用硝酸银标准溶液测定卤离子含量的沉淀滴定法)。
2FeCl2+C6H4Cl2+HCl↑。按照如图装置,在三颈烧瓶中放入162.5g无水FeCl3和225g氯苯,控制反应温度在130℃下加热3h,冷却、过滤、洗涤、干燥得到粗产品。将生成的HCl用水吸收,利用莫尔法可以测出无水FeCl3的转化率(莫尔法是用硝酸银标准溶液测定卤离子含量的沉淀滴定法)。
已知有关数据如下:
C6H5Cl | C6H4Cl2 | |
熔点/℃ | -45 | 53 |
沸点/℃ | 132 | 173 |
回答下列问题:
(1)仪器b的作用是_______。干燥管c中盛装的试剂是________。
(2)反应结束后需向反应器a中吹入干燥的氮气,其目的是_________。
(3)下列各装置(盛有蒸馏水)能代替图中虚线框内部分的是_____(填序号)。
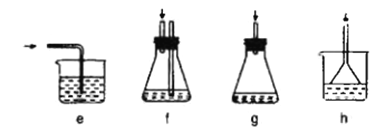
(4)从滤液中回收过量氯苯的操作是___________。
(5)将锥形瓶内溶液的pH调至6.0再加水稀释至1000mL,从中取10.0mL滴加几滴指示剂,用 0.2000mol/LAgNO3溶液进行滴定,当达到终点时,消耗22.50mLAgNO3溶液。
AgCl | AgBr | AgI | Ag2CrO4 | |
Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
颜色 | 白 | 淡黄 | 黄 | 砖红 |
①参照上表已知信息用硝酸银标准溶液滴定氯离子含量时可以作指示剂的是___(填字母)。
a.CaCl2 b.NaBr c.NaI d.K2CrO4
②滴定达终点的现象是_______
③无水FeC13的转化率a=_______%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中错误的是( )
A.构成原电池的正极和负极必须是两种不同的金属
B.原电池是将化学能转变为电能的装置
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.原电池放电时,电流的方向是从正极到负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO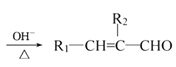 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的分子式是____,G中含氧官能团的名称是____。
(2)②的反应类型是____, F的结构简式为______。
(3)B的核磁共振氢谱有____组峰,峰面积之比为_____________。
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式:_____________。
(6)设计实验检验E中的官能团(说明实验操作步骤、现象及结论)____________
(7)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示用CuSO45H2O晶体来配制480mL 0.20mol·L-1 CuSO4溶液的几个关键实验步骤和操作,据图回答下列问题:

(1)将上述实验步骤A~F按实验过程先后次序排列 __________________,需称取CuSO45H2O 晶体的质量为__________ g。
(2)写出配制480mL0.20mol·L-1CuSO4溶液所需要用到的玻璃仪器的名称:烧杯、量筒、_______________。
(3)步骤B通常称为转移,若是配制NaOH溶液,用水溶解NaOH固体后未冷却至室温即转移,配制溶液的浓度将偏_____________(填“高”或“低”)。步骤A通常称为____________,如果俯视刻度线,配制的浓度将偏______(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图装置中,烧瓶中充满干燥气体a。将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶。a和b可能是
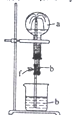
a(干燥气体) | b(液体) | |
① | NH3 | 水 |
② | CO2 | 饱和NaOH溶液 |
③ | Cl2 | 饱和食盐水 |
④ | NO2 | 水 |
⑤ | HCl | 0.1 mol·L1AgNO3溶液 |
A. ①②③ B. ①②⑤ C. ②④⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列说法中,正确的是( )
A. 1 mol Cl2作为氧化剂得到的电子数为NA
B. 在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C. 25 ℃,1.01×105Pa,64 g SO2中含有的原子数为3NA
D. 将0.1 mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
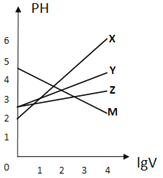
A. 相同条件下,对于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常温下pH:NaA溶液>NaB溶液
C. X是HA,M是HB
D. 若常温下浓度均为0.1mol/L的NaA和HA的溶液等体积混合,则c(A-)+c(HA)=0.2mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com