
【题目】某同学用下列装置制备并检验Cl2的性质,下列说法正确的是
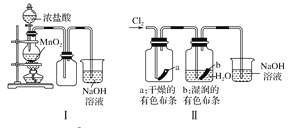
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B. Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气
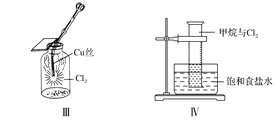
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:量筒中发生了加成反应,量筒内液面上升,量筒壁上有无色液滴出现
【答案】B
【解析】
A.稀盐酸与二氧化锰不反应;干燥的氯气没有漂白性,Cl2+H2O=HCl+HClO,HClO具有漂白性,氢氧化钠溶液与氯气反应生成氯化钠和次氯酸钠;氯气与铜反应生成棕黄色的烟;甲烷与氯气发生取代反应。
A.二氧化锰和浓盐酸在加热条件下发生氧化还原反应生成氯气,但稀盐酸与二氧化锰不反应,当盐酸浓度降低到一定程度时,反应停止,则盐酸不能完全消耗,故A错误;干燥的氯气没有漂白性,Cl2+H2O=HCl+HClO,HClO具有漂白性,氢氧化钠溶液与氯气反应生成氯化钠和次氯酸钠,所以Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气,故B正确;氯气与铜反应生成棕黄色的烟,故C错误;甲烷与氯气发生取代反应,故D错误。


科目:高中化学 来源: 题型:
【题目】某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:

(1)选用如图所示装置及药品制取CO2。打开弹簧夹,制取CO2。为了得到干燥.纯净的CO2,产生的气流应依次通过盛有_________的洗气瓶(填试剂名称)。反应结束后,关闭弹簧夹,可观察到的现象是____________________________。不能用稀硫酸代替稀盐酸,其原因是______________________________。
(2)金属钠与二氧化碳反应的实验步骤及现象如下表:
步骤 | 现象 |
将一小块金属钠在燃烧匙中点燃,迅速伸入盛有CO2的集气瓶中。充分反应,放置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
在集气瓶中加入适量蒸馏水,振荡.过滤 | 滤纸上留下黑色固体,滤液为无色溶液 |
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红:向第二支试管中滴加澄清石灰水,溶液变浑浊。
据此推断,白色物质的主要成分是________(填标号)。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是________________。
③本实验中金属钠与二氧化碳反应的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,前者是纯净物,后者是混合物的是( )
A. 水煤气、铝热剂 B. 盐酸、磷酸钙
C. 硫酸铜晶体、漂白粉 D. 玻璃、含Fe为70%的氧化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. 加入催化剂有利于氨的合成
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】土壤也是一种胶体,研究发现土壤中的胶体粒子主要带负电荷。化肥施入土壤中,往往先被土壤胶粒吸附固定下来,再被作物吸收。在水田里使用下列氮肥时,哪一种容易造成肥效降低( )
A. 碳酸氢铵(NH4HCO3 B. 氯化铵(NH4Cl)
C. 硫酸铵〔(NH4)2SO4〕 D. 硝酸铵(NH4NO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体X投入过量的Y中,能生成蓝色沉淀并放出一种无色气体,该气体能燃烧,不易溶于水,则X和Y分别可能是( )
A.Na和AlCl3溶液B.Al和NaOH溶液
C.Na2O2和CuSO4溶液D.Na和CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.晶体硅常用于制作光导纤维
B.钠能从溶液中置换出金属活动顺序表中钠后面的金属
C.蒸馏时,冷凝水从冷凝管上管口进,由下管口出
D.碘水中萃取碘时,往分液漏斗中先后加入碘水和四氯化碳,充分振荡静置后分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是生命必要的元素,也是人类最早使用的金属之一,西汉时期《淮南万毕术》里就有“曾青得铁,则化为铜”的记载,曾青可能是碳酸铜一类物质,把其溶于酸中得溶液,当把铁粉投入此溶液即可得铜。
(1)根据学过的化学知识,写出该过程的离子方程式:________。
(2)在化学反应中,铜元素可表现为0、+1、+2。Cu2+ 的未成对电子数有______个,向硫酸铜溶液中加入过量的氨水可以得到 [Cu(NH3)4]SO4 溶液,[Cu(NH3)4]2+的结构简式为___。
(3)向[Cu(NH3)4]SO4 水溶液中通入SO2 气体至溶液呈微酸性,析出白色沉淀CuNH4SO3。反应化学方程式为 _____________。
(4)CuNH4SO3 与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途,写出该反应的离子方程式________,若该反应在密闭容器中进行,且酸量充足,计算反应物中Cu元素变成超细粉末Cu的转化率_______,理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com