
【题目】(1)按图装置进行实验。请回答下列问题:

①以下叙述错误的是_______________(填字母)。
A.铜片是正极,表面有气泡产生
B.装置中存在“化学能→电能→光能”的转化
C.外电路中电流方向Zn→Cu
D.溶液中SO42-向铜片方向移动
②实验发现不仅在铜片上有气泡产生,在锌片上也有气泡产生。分析锌片上产生气泡的原因是_______________________。
③实验中当负极材料消耗质量为2.6g时,则电路中转移电子数为___________。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①电池工作时,空气从_____口通入(填“A”或“B”);
②若使用的燃料为氢气(H2),a极的电极反应式为_____________________。
【答案】CD 锌与稀硫酸直接反应生成了氢气 0.08NA B H2-2e-+2OH-=4H2O
【解析】
(1)该装置为原电池装置,电池总反应为Zn+H2SO4=ZnSO4+H2↑,所以Zn为负极,Cu为正极;
(2)根据电子的流向可知a为负极,b为正极。
(1)①A.根据分析可知铜片为正极,氢离子得电子生成氢气,所以有气泡生成,故A正确;
B.原电池可以将化学能转化为电能,电能通过LED灯转化为光能,故B正确;
C.外电路中电流由正极流向负极,即Cu→Zn,故C错误;
D.电解质溶液中阴离子流向负极,所以硫酸根流向锌片,故D错误;
综上所述选CD;
②锌与稀硫酸直接反应生成了氢气,所以锌片上也产生气泡;
③负极发生Zn-2e-=Zn2+,2.6g锌的物质的量为![]() =0.04mol,根据电极方程式可知转移的电子数为0.08NA;
=0.04mol,根据电极方程式可知转移的电子数为0.08NA;
(2)①燃料电池中,氧气发生还原反应,为正极,所以空气从B口通入;
②若燃料为氢气,则氢气发生氧化反应,A口通入a极反应,电解质溶液为碱性,所以电极反应式为H2-2e-+2OH-=4H2O。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列七种有机物中:
A.CH4 B.CH2=CH2 C.![]()
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
(1)酸性比碳酸强的是______(填字母编号,下同).
(2)易发生银镜反应的是______.(3)具有正四面体结构的是______.
(4)通常用于检验碘单质的是______.(5)可用于合成聚乙烯塑料的是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸是无色晶体,无臭、味极酸,分子结构如图所示。广泛用于食品业、化妆业等。其钙盐在冷水中比在热水中易溶解。下列有关柠檬酸的说法不正确的是
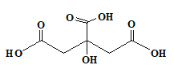
A. 易溶于水,其分子式为C6H8O7
B. 1mol该物质与足量的钠反应最多生成2molH2
C. 利用钙盐溶解性重结晶分离
D. 能作食品抗氧化剂,补酸剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前中国已经通过自主创新成功研发出第一台锌溴液流储能系统,实现了锌溴电池的隔膜、极板、电解液等关键材料自主生产。锌溴电池的原理装置图如图所示,下列说法错误的是( )

A.充电时电极石墨棒A连接电源的正极
B.放电过程中阴离子通过隔膜从正极区移向负极区
C.放电时负极反应为2Br-—2e-=Br2
D.放电时右侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、铁、镁等元素在生产生活中有广泛的用途,完成下列填空:
Ⅰ钠的重要化合物
(1)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯气需要0.56g硫代硫酸钠,反应的离子方程式为______。
(2)除去Al2O3中混有的Fe2O3,可将混合物溶于过量的盐酸,再加入Na2CO3调节pH使Fe3+沉淀完全而Al3+不沉淀,用化学用语及相应的离子方程式解释加入Na2CO3的目的______。
Ⅱ铁的重要化合物
(3)磷酸铁(FePO42H2O是难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
①称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是______。
②向滤液中加入一定量H2O2氧化Fe2+,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、______和______。
③将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO42H2O.若反应得到的FePO4H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为______。
Ⅲ镁的重要化合物
(4)氧化镁和碳粉与氯气在一定条件下反应可制备氯化镁,若尾气可用足量的氢氧化钠溶液完全吸收,则生成的盐为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组成员为研究金属铜与强酸的反应 ,将6.4g铜粉分为两等份,进行了如下实验,请完成有关计算。
(1)取其中一份铜粉投入200mL氢离子浓度为 1molL-1 硫酸和硝酸混合液中,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前混合溶液中硫酸的物质的量浓度为_________(写出计算过程)。
(2)用NaOH溶液吸收氮氧化物是防止NO2污染的一种方法。原理为2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O。取另一份铜粉溶于过量的硝酸溶液,假设硝酸的还原产物只有一氧化氮和二氧化氮,生成的混合气体能被amol NaOH溶液完全吸收,试讨论a的取值范围:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化锡(SnI4)是一种橙黄色结晶,熔点为 144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿、四氯化碳等,遇水易水解,常用作分析试剂和有机合成试剂。实验室制备四氯化锡的主要步骤如下:
步骤1:将一定量锡、碘和四氯化碳加入干燥的烧瓶中,烧瓶上安装如图装置Ⅰ和Ⅱ。

步骤2:缓慢加热烧瓶,待反应停止后,取下冷凝管,趁热迅速进行过滤除去未反应的锡。用热的四氯化碳洗涤漏斗上的残留物,合并滤液和洗液,用冰水浴冷却,减压过滤分离。
步骤3:滤下的母液蒸发浓缩后冷却,再回收晶体。
请回答下列问题
(1)图中装置II的仪器名称为___________,该装置的主要作用是____________。
(2)减压过滤的操作有①将含晶体的溶液倒入漏斗,②将滤纸放入漏斗并用水润湿,③微开水龙头,④开大水龙头,⑤关闭水龙头,⑥拆下橡皮管。正确的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )

A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.四种元素的单质中,Z单质的熔、沸点最低
D.W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物D的一种合成路线如下:
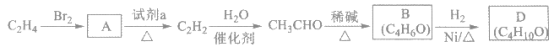
已知:![]()
 +H2O(R、R'表示烃基或氢)
+H2O(R、R'表示烃基或氢)
(1)由C2H4生成A的化学方程式是___________。
(2)试剂a是________。
(3)写出B中所含官能团的名称________。
(4)有机物D的结构简式是________。
(5)请以乙烯为起始原料,以CH3CH=CHCOOH为目标产物,结合已知信息选择必要的无机试剂,写出合成路线。_______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com