
【题目】某课外兴趣小组成员为研究金属铜与强酸的反应 ,将6.4g铜粉分为两等份,进行了如下实验,请完成有关计算。
(1)取其中一份铜粉投入200mL氢离子浓度为 1molL-1 硫酸和硝酸混合液中,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前混合溶液中硫酸的物质的量浓度为_________(写出计算过程)。
(2)用NaOH溶液吸收氮氧化物是防止NO2污染的一种方法。原理为2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O。取另一份铜粉溶于过量的硝酸溶液,假设硝酸的还原产物只有一氧化氮和二氧化氮,生成的混合气体能被amol NaOH溶液完全吸收,试讨论a的取值范围:_____。
【答案】0.45mol·L-1 a≥0.1
【解析】
(1)200mL氢离子浓度为1mol·L-1的混合液中含有氢离子的物质的量为:n(H+)=0.2L×1mol·L-1=0.2mol,
3.2g铜粉物质的量为:![]() =0.05mol,NO的物质的量为:
=0.05mol,NO的物质的量为:![]() =0.02mol,根据3Cu+8H++2NO3-=3Cu2++2NO↑+3H2O可知,生成0.02molNO,需要铜0.03mol、H+为0.04mol,所以铜、H+过量,硝酸不足,硝酸完全反应,
=0.02mol,根据3Cu+8H++2NO3-=3Cu2++2NO↑+3H2O可知,生成0.02molNO,需要铜0.03mol、H+为0.04mol,所以铜、H+过量,硝酸不足,硝酸完全反应,
根据氮元素守恒可知,溶液中n(HNO3)=n(NO)=0.02mol,0.02mol硝酸中含有0.02mol氢离子,则硫酸中含有的氢离子的物质的量为:0.2mol-0.02mol=0.18mol,则硫酸的物质的量浓度为: =0.45mol·L-1;
=0.45mol·L-1;
故答案为:0.45mol·L-1;
(2)0.05molCu如全生成NO,根据3Cu+8H++2NO3-=3Cu2++2NO↑+3H2O得NO为![]() =
=![]() ,0.05molCu如全生成NO2,根据Cu+4H++2NO3-=Cu2++2NO2↑+2H2O得NO2为
,0.05molCu如全生成NO2,根据Cu+4H++2NO3-=Cu2++2NO2↑+2H2O得NO2为![]() =0.1mol,根据2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O,无论生成NaNO3 还是 NaNO2,Na与N的物质的量比为1:1,有1mol一氧化氮和二氧化氮的混合气体,就需要1molNaOH,生成的混合气体能被amol NaOH溶液完全吸收,a的取值范围:a≥0.1;
=0.1mol,根据2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O,无论生成NaNO3 还是 NaNO2,Na与N的物质的量比为1:1,有1mol一氧化氮和二氧化氮的混合气体,就需要1molNaOH,生成的混合气体能被amol NaOH溶液完全吸收,a的取值范围:a≥0.1;
故答案为:a≥0.1。


科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能一步实现的是
A.NaCl(aq) ![]() NaHCO3
NaHCO3![]() NaCO3
NaCO3
B.Al![]() NaAlO2
NaAlO2![]() AlCl3(aq)
AlCl3(aq) ![]() AlCl3(s)
AlCl3(s)
C.Fe![]() FeCl2
FeCl2![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3
D.H2SO4(aq) ![]() SO2
SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO3
(NH4)2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 27g铝箔在酒精灯上充分加热反应转移电子总数是3NA
B. 2.0gCO2与SO2的混合气体分子中,含有的质子数为NA
C. 25℃时,Ksp(BaSO4)=1×1010,则BaSO4饱和溶液中Ba2+数目为1×105NA
D. 7.8gNa2O2中含有的阴、阳离子的总数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生验证浓硫酸性质的实验如图。下列叙述错误的是

A.反应一段时间后,b处滤纸条褪色
B.蘸有NaOH溶液的棉花团作用是吸收多余的SO2,防止污染空气
C.化学反应方程式:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
D.硫酸型酸雨形成的可能原因是:SO2+H2O![]() H2SO3;O2+2H2SO3=2H2SO4
H2SO3;O2+2H2SO3=2H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按图装置进行实验。请回答下列问题:

①以下叙述错误的是_______________(填字母)。
A.铜片是正极,表面有气泡产生
B.装置中存在“化学能→电能→光能”的转化
C.外电路中电流方向Zn→Cu
D.溶液中SO42-向铜片方向移动
②实验发现不仅在铜片上有气泡产生,在锌片上也有气泡产生。分析锌片上产生气泡的原因是_______________________。
③实验中当负极材料消耗质量为2.6g时,则电路中转移电子数为___________。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①电池工作时,空气从_____口通入(填“A”或“B”);
②若使用的燃料为氢气(H2),a极的电极反应式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸在水中电离方程式可表示为:CH3COOH![]() CH3COO—+H+ ΔH>0,下列操作能使H+ 浓度增大的是 ( )
CH3COO—+H+ ΔH>0,下列操作能使H+ 浓度增大的是 ( )
A. 加入少量NaOH固体 B. 小心加热升温10oC C. 加入锌粉 D. 加入固体CH3COONa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“太阳水”电池装置如图所示,该电池由三个电极组成,其中 a 为TiO2电极,b 为Pt 电极,c 为 WO3 电极,电解质溶液为 pH=3 的 Li2SO4-H2SO4 溶液。锂离子交换膜将电池分为 A、B 两个区,A 区与大气相通,B 区为封闭体系并有 N2 保护。下列关于该电池的说法错误的是
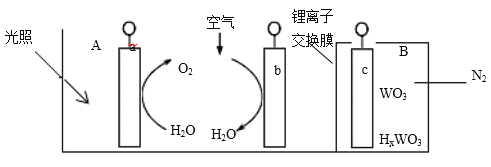
A.若用导线连接a、c,则 a 为负极,该电极附近 pH 减小
B.若用导线连接 a、c,则 c 电极的电极反应式为HxWO3-xe-=WO3+ xH+
C.若用导线连接 b、c,b 电极的电极反应式为 O2+4H++4e-=2H2O
D.利用该装置,可实现太阳能向电能转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的性质与原子结构、元素在周期表中的位置有着密切的关系。回答下列问题:
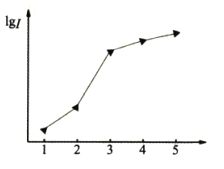
(1)如图表示某短周期元素X的前五级电离能(I)的对数值,试推测并写出X的元素符号___。
(2)化合物甲与SO2所含元素种类相同,两者互为等电子体,请写出甲的化学式___,甲分子中心原子的杂化类型是___。
(3)配位化学创始人维尔纳发现,将1mo1CoC13·5NH3(紫红色)和1mo1CoC134NH3(绿色)溶于水,加入AgNO3溶液,立即沉淀的AgCl分别为2mo1、1mol。则紫红色配合物中配离子的化学式为___,绿色配合物中Co的配位数为___。
(4)某稀土元素M的氧化物晶体为立方晶胞,其结构如图所示,图中小球代表氧离子,大球代表M离子。
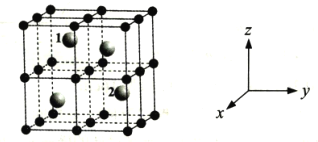
①写出该氧化物的化学式___。
②己知该晶体密度为ρg·cm-3,晶胞参数为anm,NA为阿伏加德罗常数的值。则M的相对原子质量Mr=___(用含ρ、a等的代数式表示);
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1(M原子)的坐标为(![]() ,
,![]() ,
,![]() ),则原子2(M原子)的坐标为___。
),则原子2(M原子)的坐标为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com