
【题目】常温下,下列叙述正确的是( )
A.pH=a的氨水,稀释10倍后,其pH=b,则a<b+1
B.在滴有酚酞溶液的氨水中,加入NH4Cl溶液恰好无色,则此时溶液的pH<7
C.向10mL0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中,![]() 将减小
将减小
D.向10mLpH=11的氨水中加入10mLpH=3的H2SO4溶液,混合液pH=7
【答案】AC
【解析】
A.pH=a的强碱溶液稀释10n倍,溶液的新pH=a-n(pH﹥7),一水合氨为弱碱,加水稀释促进其电离,相比强碱而言,稀释过程还产生一定的OH-,稀释后溶液碱性比相同情况下的强碱强,则![]() 的氨水稀释101倍后,其新pH﹥a-1,即b﹥a-1,则
的氨水稀释101倍后,其新pH﹥a-1,即b﹥a-1,则![]() ,A正确;
,A正确;
B.酚酞的变色范围为![]() ,所以在滴有酚酞试液的氨水中,加入稀盐酸至溶液恰好无色,此时溶液的pH﹤8.2,B错误;
,所以在滴有酚酞试液的氨水中,加入稀盐酸至溶液恰好无色,此时溶液的pH﹤8.2,B错误;
C.一水合氨的电离平衡Kb=![]() ,温度不变则Kb不变,
,温度不变则Kb不变,![]() 不变,向
不变,向![]() 溶液中滴加少量氨水,但是c(OH-)增大,所以
溶液中滴加少量氨水,但是c(OH-)增大,所以![]() 减小,C正确;
减小,C正确;
D.向![]() 的氨水中加入
的氨水中加入![]() 的
的![]() 溶液,由于一水合氨为弱碱,反应过程还会产生大量OH-,故混合液呈碱性,则混合液的
溶液,由于一水合氨为弱碱,反应过程还会产生大量OH-,故混合液呈碱性,则混合液的![]() ,D错误。
,D错误。
答案选AC。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z三种有机物互为同系物,下列有关说法错误的是( )
A.若X为![]() ,则Y不可能是
,则Y不可能是![]()
B.若X是甲醇、Y是乙醇,则Z一定能发生消去反应
C.若X为苯,Y为甲苯,则Z的相对分子质量一定不低于106
D.若X、Y均是饱和一元醛,则Z的分子式一定不是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按如图所示转化进行综合利用(部分反应条件及产物没有列出)。
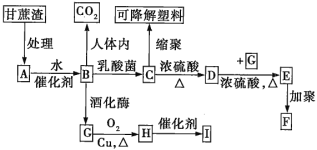
其中B是A水解的最终产物;C的分子式为C3H6O3,一定条件下2个C分子分子间脱去2分子水可生成一种六元环状化合物;D可使溴水褪色;H的三聚物I也是一种六元环状化合物。
提示:葡萄糖在乳酸菌作用下生成乳酸(![]() )。
)。
(1)C→D的反应类型为__,D→E的反应类型为__。
(2)写出A→B反应的化学方程式:_。
(3)H分子中所含官能团的名称是__,实验室中常用于检验该官能团的试剂的名称是_(只写一种)。
(4)写出下列物质的结构简式:高分子化合物F__;六元环状化合物I_。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如图所示装置,可发现电流计指针偏转,M棒变粗,N棒变细.下表所列的M、N、P对应物质可构成该装置的是( )
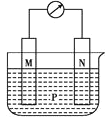
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
③CH4(g)+2O2(g)=2H2O(l)+CO2(g) ΔH=-890kJ·mol-1
(1)已知H—H键的键能为436kJ·mol-1,O=O键的键能为496kJ·mol-1,H—O键的键能为463kJ·mol-1,根据上述数据通过键能可直接计算出反应___(填反应序号)的焓变,由反应①②可得出反应比H2O(l)=H2O(g)的焓变ΔH=___。
(2)根据题干可计算出CO2(g)+4H2(g)=CH4(g)+2H2O(g)的焓变ΔH=___。
(3)在①②③三个热化学方程式中,可表示燃烧热的热化学方程式的是___(填序号)。标准状况下,取甲烷和氢气的混合气体11.2L,完全燃烧后恢复到常温,放出的热量为263.8kJ,则混合气体中甲烷和氢气的体积比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某油脂A,在稀硫酸作催化剂的条件下水解,生成脂肪酸和多元醇B,B和硝酸在浓硫酸作用下通过酯化反应生成有机物D。
(1)写出油脂A在稀硫酸作催化剂的条件下水解的化学方程式:__。
(2)已知D由C、H、O、N四种元素组成,相对分子质量为227,C、H、N的质量分数分别为15.86%、2.20%和18.50%,则D的分子式是__,B→D的化学方程式是__。
(3)C是B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列数据:
物质 | 熔点/℃ | 沸点/℃ | 密度/ |
乙醇 |
| 78.3 | 0.79 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 |
| 77 | 0.90 |
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制![]() 浓硫酸、
浓硫酸、![]() 乙醇(含
乙醇(含![]() )和
)和![]() 乙酸的混合溶液。
乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热![]() 。
。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
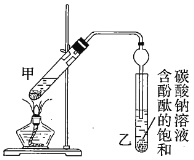
(1)配制①中混合溶液的方法为_______________________________;反应中浓硫酸的作用是____________________________;写出制取乙酸乙酯的反应的化学方程式:____________________________(标出![]() )。
)。
(2)上述实验中饱和碳酸钠溶液的作用是________(填字母)。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要原因是____________________________;步骤③所观察到的现象是_______________________________________;欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有___________;分离时,乙酸乙酯应从仪器_____________(填“下口放”或“上口倒”)出。
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如下表:
实验 | 乙醇/ | 乙酸/ | 乙酸乙酯/ |
① | 2 | 2 | 1.33 |
② | 3 | 2 | 1.57 |
③ | 4 | 2 | x |
④ | 5 | 2 | 1.76 |
⑤ | 2 | 3 | 1.55 |
表中数据x的范围是__________________;实验①②⑤探究的是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,结论错误的是
A.硬度:金刚石>碳化硅>晶体硅
B.离子半径:S2->Cl->Na+>O2-
C.熔点:NaF>NaCl>NaBr>NaI
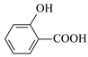
D.沸点:![]() >
>
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com