
【题目】铬铁矿的主要成分可表示为FeOCr2O3 , 还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图: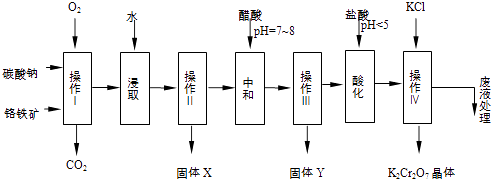
已知:
①4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 ![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
根据题意回答下列问题:
(1)操作I在常温下该反应速度极慢,下列措施中能使反应速率增大的是 .
A.升高温度
B.通入过量的空气
C.将原料粉碎
D.增加纯碱的用量
(2)固体X中主要含有(填写化学式);
(3)酸化步骤用盐酸调节溶液pH<5,并煮沸其目的是 . (离子方程式表示)
(4)操作 iv有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、、、洗涤、干燥.
(5)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.该反应在溶液中能发生的理由是 . (文字说明)
物质 | 溶解度/(g/100g水) | ||
0°C | 40°C | 80°C | |
KCl | 28 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
Na2Cr2O7 | 163 | 215 | 376 |
(6)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量(填写试剂)、溶解、过滤、再(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为(用含m、n的代数式表示).
【答案】
(1)ABC
(2)Fe2O3、MgO
(3)Cr2O72﹣+H2O═2CrO42﹣+2H+
(4)冷却结晶;过滤
(5)K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小)
(6)NaOH溶液;通入过量二氧化碳;![]()
【解析】解:(1)A.升高温度,可以加快反应速率,故A正确; B.通入过量的空气,增大了氧气的量,可以加快反应速率,故B正确; C.将原料粉碎,增大了接触面积,可以加快反应速率,故C正确;D.纯碱是固体,不涉及浓度问题,所以改变纯碱的量,不能改变反应速率,故D错误;所以答案是:ABC;(2)铬铁矿的主要成分可表示为FeOCr2O3 , 还含有MgO、Al2O3、Fe2O3等杂质,加入氧气和碳酸钠,发生反应为:4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2↑;Na2CO3+Al2O3
8Na2CrO4+2Fe2O3+8CO2↑;Na2CO3+Al2O3 ![]() 2NaAlO2+CO2↑;Cr2O72﹣+H2O2CrO42﹣+2H+ , 操作Ⅰ是过滤得到固体X为Fe2O3、MgO,所以答案是:Fe2O3、MgO;(3)酸化步骤用醋酸调节溶液pH<5,依据流程图中物质的转化和制备目的可知,结合反应平衡Cr2O72﹣+H2O2CrO42﹣+2H+ , 加入酸,氢离子浓度增大,平衡左移,作用是使CrO42﹣转化为Cr2O72﹣ , 所以答案是:Cr2O72﹣+H2O═2CrO42﹣+2H+;(4)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩,冷却结晶、过滤、洗涤、干燥得到晶体,
2NaAlO2+CO2↑;Cr2O72﹣+H2O2CrO42﹣+2H+ , 操作Ⅰ是过滤得到固体X为Fe2O3、MgO,所以答案是:Fe2O3、MgO;(3)酸化步骤用醋酸调节溶液pH<5,依据流程图中物质的转化和制备目的可知,结合反应平衡Cr2O72﹣+H2O2CrO42﹣+2H+ , 加入酸,氢离子浓度增大,平衡左移,作用是使CrO42﹣转化为Cr2O72﹣ , 所以答案是:Cr2O72﹣+H2O═2CrO42﹣+2H+;(4)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩,冷却结晶、过滤、洗涤、干燥得到晶体,
所以答案是:冷却结晶;过滤;(5)依据图表物质的溶解度分析对比,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl;说明K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小),所以答案是:K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小);(6)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是先利用氢氧化铝的两性,用氢氧化钠溶液溶解氢氧化铝过滤得到滤液中通入二氧化碳生成氢氧化铝沉淀,灼烧干燥得到氧化铝干燥固体m g,依据铝元素守恒计算,样品中氢氧化铝的质量分数= ![]() ×100%=
×100%= ![]() ,
,
所以答案是:NaOH溶液;通入过量二氧化碳; ![]() .
.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( ) 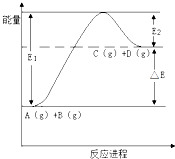
A.该反应是放热反应
B.加入催化剂后,反应加快,△E减小
C.反应物的总键能大于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(A)=0.5mol·(L· s)-1 B. v(B)=0.3 mol·(L· s)-1
C. v(C)=0.8 mol·(L· s)-1 D. v(D)=1 mol·(L· s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.制备铜氨纤维时,取出稀盐酸中的生成物,用水洗涤,得到蓝色的铜氨纤维
B.天然气的主要成分是甲烷,不同地区天然气中甲烷含量不同
C.长久存放的氯水逐渐转变为很稀的盐酸
D.在燃烧木柴时,将木材架空,木材会燃烧的更旺
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应最终一定有+3价铁生成的是( )
①过量的Fe与![]() 反应 ②Fe与过量稀硫酸反应后,再向其中加
反应 ②Fe与过量稀硫酸反应后,再向其中加![]() ③
③![]() 溶液中加少量盐酸 ④把Fe和
溶液中加少量盐酸 ④把Fe和![]() 的混合物溶于盐酸中
的混合物溶于盐酸中
A.只有① B.只有①② C.只有①②③ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构的叙述中不正确的是( )
A.乙烯、溴苯分子中的所有原子均共平面
B.在有机物分子中,含有的氢原子个数一定是偶数
C.![]() 与
与 ![]() 属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图A、B、C是某课外活动小组设计的制取氨气并进行喷泉实验的三组装置示意图,制取NH3选用试剂如图所示,回答下列问题:
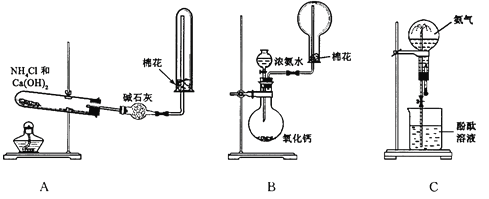
(1)用A图所示的装置可制备干燥的NH3
①反应的化学方程式为:________________________________________。装置中收集NH3的试管口放置棉花团的作用是_________________________________________。
②干燥管中干燥剂能否改用无水CaCl2___________,理由是_______________________。
(2)用B图所示的装置可快速制取较大量NH3拟作喷泉实验。根据B图所示的装置及试剂回答下列问题:
①用化学方程式表示浓氨水滴入CaO中有大量NH3逸出的过程:_________________________
②检验NH3是否收集满的实验方法是:______________________________________________。
(3)用C图所示的装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发喷泉的操作是___________________________,若实验结束后溶液充满整个烧瓶,则氨水的浓度为_______________________(假设实验在标况下进行)。若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的___________(填“几分之几”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分离是化学研究中常用的方法,填写分离下列物质时使用的方法(不必叙述操作细节).
(1)两种互不相溶的液体的分离 .
(2)固体和液体的分离 .
(3)含固体溶质的溶液中除去部分溶剂 .
(4)胶体中分离出可溶电解质 .
(5)几种沸点相差较大的互溶液体的分离 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com