
| A. | 氧化性:MnO4-<Cl2<Fe3+<I2 | |
| B. | 还原性:Fe2+>I->Cl- | |
| C. | FeCl3能使湿润的淀粉碘化钾试纸变蓝 | |
| D. | 反应①中只体现盐酸的还原性 |
分析 A、根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性;
B、根据氧化还原反应中还原剂的还原性强于还原产物的还原性;
C、由反应2KI+2FeCl3═2KCl+I2+2FeCl2可知,FeCl3能碘化钾反应生成碘单质,碘单质与淀粉变蓝;
D、反应2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O中,氯的化合价部分变化,所以盐酸体现酸性和还原性.
解答 解:A、①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,氧化性:KMnO4>Cl2;
②Cl2+2FeCl2═2FeCl3,氧化性:Cl2>FeCl3;
③2KI+2FeCl3═2KCl+I2+2FeCl2,氧化性:FeCl3>I2;所以氧化性强弱的顺序为:KMnO4>Cl2>FeCl3>I2,故A错误;
B、①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,还原性:HCl>MnCl2;
②Cl2+2FeCl2═2FeCl3,还原性:Fe2+>Cl-;
③2KI+2FeCl3═2KCl+I2+2FeCl2,还原性:I->Fe2+,所以还原性强弱的顺序为:I->Fe2+>Cl-,故B错误;
C、由反应2KI+2FeCl3═2KCl+I2+2FeCl2可知,FeCl3能碘化钾反应生成碘单质,碘单质与淀粉变蓝,故C正确;
D、反应2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O中,氯的化合价部分变化,所以盐酸体现酸性和还原性,所以反应①中只体现盐酸的还原性,故D错误;
故选C.
点评 本题考查氧化性强弱判断方法,明确氧化性、还原性判断方法即可解答,会正确判断氧化剂、氧化产物是解本题关键,知道常见元素化合价,题目难度不大.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了节约应将实验过程中取用的剩余药品放回原试剂瓶 | |
| B. | 在汽油罐上所贴的危险化学品标志内容是:遇湿易燃物品 | |
| C. | 酒精着火,迅速用湿抹布或沙子盖灭 | |
| D. | 氢氧化钠溶液溅入眼中,应立即用大量水冲洗,再用稀盐酸冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{576V}$ mol•L-1 | B. | $\frac{a}{125}$ mol•L-1 | C. | $\frac{250a}{36V}$mol•L-1 | D. | $\frac{250a}{48V}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶于水后能电离出H+的化合物都是酸 | |
| B. | BaSO4不溶于水,故BaSO4不是电解质 | |
| C. | CO2溶于水后溶液能导电,故CO2是电解质 | |
| D. | 尽管NaCl固体不导电,但NaCl是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密闭、低温是存放氨水的必要条件 | |
| B. | 实验室常用排饱和食盐水法收集氯气 | |
| C. | 打开汽水瓶时,有大量气泡冒出 | |
| D. | 已知合成氨的反应为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol,工业上采用较高温度和使用催化剂以提高氨气的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH(CH3)CH2CH3 2-甲基丁烷 | B. | 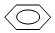 间二甲苯 间二甲苯 | ||
| C. | CH3CH2CH2CH2OH 1-羟基丁烷 | D. | 2-甲基-2-丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾是气溶胶,在阳光下可观察到丁达尔效应 | |
| B. | 预制备Fe(OH)3胶体,向盛有沸水的烧杯中加入FeCl3饱和溶液煮沸得红褐色沉淀 | |
| C. | 用石膏或卤水点制豆腐利用了胶体的性质 | |
| D. | 用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
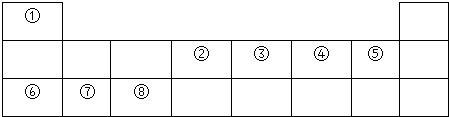
 .
. .
. ,其晶体类型属于分子晶体,④与⑥形成的原子个数比为1:1的化合物的电子式是
,其晶体类型属于分子晶体,④与⑥形成的原子个数比为1:1的化合物的电子式是 ,其晶体类型属于离子晶体.
,其晶体类型属于离子晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com