
【题目】下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性)
B. 在加热条件下铜与浓硫酸反应(强氧化性、酸性)
C. 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D. 浓硫酸可用来干燥某些气体(脱水性)
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】下列实验方案中不能达到相应实验目的是( )
A | B | C | D | |
方案 |
|
|
|
|
目的 | 探究浓度对化学反应速率的影响 | 制备氨气 | 室温下比较NaHCO3和Na2CO3的溶解度 | 探究温度对化学平衡的影响 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%,密度为1.84g/cm3的浓硫酸来配制200ml 1mol/L的稀硫酸,可供选择的仪器有:①量筒 ②烧杯 ③胶头滴管 ④玻璃棒.
(1)除上述仪器中,配制过程中还差的有 .
(2)计算所需浓硫酸的体积为 . 现有①5ml ②10ml ③20ml④50ml四种规格的量筒,最好选用 . (填代号)
(3)在配制过程中,下列操作可引起所配溶液浓度偏低的有 . (填代号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到定量瓶中.
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
⑤定容量,仰视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的一部分如图,请参照元素①~⑨在表中的位置,用化学用语回答下列问题: 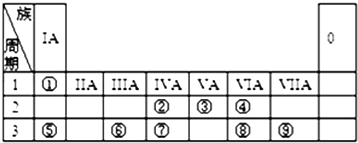
(1)已知②的一种核素中子数为8,则其气态氢化物的摩尔质量为
(2)①②⑤⑥的原子半径由大到小的顺序为(填元素符号);⑦⑧⑨的最高价含氧酸的酸性由强到弱的顺序是(填化学式): .
(3)⑥的最高价氧化物可以与⑤的最高价氧化物对应水化物的溶液能发生反应,该反应的化学方程式为:
(4)X、Y是中学化学中的常见物质,X、Y分别由元素④、⑤和②、④组成,X与Y的反应是潜水艇和呼吸面具中氧气的来源.X的电子式是 , Y中含有的化学键类型是 .
(5)某研究性学习小组设计了一组实验来探究元素周期律.甲同学设计了如图装置来一次性完成的②、⑦非金属性强弱比较的实验研究. 
甲同学设计实验的依据是;其中装置B中所盛试剂的作用为;C中反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式不正确的是( )
A.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+
B.电解熔融氧化铝:2Al2O3(熔融) ![]() 4Al+3O2↑
4Al+3O2↑
C.NaHCO3溶液与稀H2SO4反应:HCO3﹣+H+═H2O+CO2↑
D.向Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验填空题:实验室现要制取一瓶纯净干燥的氯气.现有如图仪器和药品可供使用: 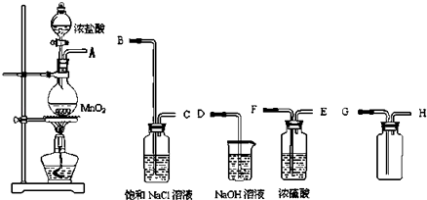
(1)实验室制取氯气的原理:;其中HCl所表现的性质是 .
(2)连接上述仪器的正确顺序是(填各接口处的字母)接 , 接 , 接 , 接 .
(3)在以上装置中,分别盛装了一些溶液,试说明所装溶液的作用.饱和食盐水的作用是;浓硫酸的作用是;氢氧化钠的作用是 .
(4)盛装NaOH溶液的试剂瓶中发生的化学反应为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学研究中,往往可以通过观察现象认识物质变化的情况.请分析以下一组有现象变化的化学反应.
实验 | 试剂及操作 | 现象 | |
试管 | 滴管 | ||
| 饱和Na2SlO3溶液(含2滴酚酞) | 先滴加1.0mL0.5molL﹣1NaOH溶液:再滴加1.5mL1.0molL﹣1H2SO4溶液 | Ⅰ.红色溶液中出现胶状沉淀 |
0.1molL﹣1AlCl3溶液 | Ⅱ.加碱时 ;加酸时产生白色沉淀,又逐渐溶解直至消失 | ||
0.1molL﹣1Fe(NO3)2溶液 | Ⅲ.加碱时 ;加酸后溶液变为黄色 | ||
新制饱和氯水 | Ⅳ.加碱时溶液变为无色;加酸后无色溶液变为浅黄绿色 | ||
(1)用离子方程式解释现象I中出现胶状沉淀的原因: .
(2)II中加碱时出现的现象是 , 此现象说明溶液中发生反应的离子方程式是 .
(3)III中加碱时出现的现象是 .
(4)用离子方程式解释IV中加碱时出现的现象 .
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验.
实验 | 试剂及操作 | 现象 | |
试管 | 滴管 | ||
| 0.1 molL﹣1 Fe(NO3)2溶液 | 先滴加1.5 mL 1.0 molL﹣1 H2SO4溶液; | V.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 |
①探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL 0.1molL﹣1Fe(NO3)2溶液中 , 溶液立即变红,说明溶液中含Fe3+ , 证明加酸时溶液中发生了反应.
②推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1molL﹣1 Fe(NO3)2溶液中的Fe2+被NO3﹣氧化;
b.(用离子方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义,对于密闭 容器中的反应:N2(g)+3H2(g)2NH3(g)(正反应为放热反应),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( ) 
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d (t1时刻)和点e (t2时刻)处n (N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比图中d点的值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,各原子最外层电子数之和为10.A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述不正确的是( )
A.D元素处于元素周期表中第三周期ⅣA族
B.四种元素的原子半径:A<B<D<C
C.B,D的氧化物均为酸性氧化物
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com