
| A.与水反应有乙炔生成 | B.与水反应有Mg(OH)2生成 |
| C.有C-C键 | D.有C22-离子 |
 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源:不详 题型:单选题
A.CO32-+H2O HCO3-+OH- 热的纯碱溶液清洗油污 HCO3-+OH- 热的纯碱溶液清洗油污 |
B.Al3++3H2O Al(OH)3(胶体)+3H+ 明矾净水 Al(OH)3(胶体)+3H+ 明矾净水 |
| C.Al3++3HCO3-=Al(OH)3↓+3CO2↑ 泡沫灭火器灭火 |
| D.SnCl2+H2O=Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c (Na+)= c (HCO3-)+ c (CO32-)+ c (H2CO3) |
| B.c(Na+)+ c (H+)=" c" (HCO3-)+ c (CO32-)+ c (OH-) |
| C.HCO3-的水解程度大于HCO3-的电离程度 |
| D.c (H+) + c(H2CO3)=c (OH-)+ c(CO32-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 )
) )>c(NH
)>c(NH )>c(OH-)=c(H+)
)>c(OH-)=c(H+)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)=c(CH3COO-)+c(CH3COOH) |
| B.c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C.c(Na+)+c(OH-)= c(CH3COO-)+c(H+) |
| D.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3溶液: C(OH—)+ C(H+)= C(HCO3—)+2 C(H2CO3) |
B.0.1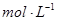  溶液: 溶液: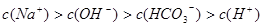 |
C.室温下,向0.01 溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: |
D.25℃时, .浓度均为0.1 .浓度均为0.1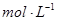 的 的 混合溶液: 混合溶液: |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com