
 H+ + CO32- HCO3- + H2O
H+ + CO32- HCO3- + H2O  OH- + H2CO3
OH- + H2CO3 H+ + CO32-、HCO3- + H2O
H+ + CO32-、HCO3- + H2O  OH- + H2CO3;其电荷守恒和物料守恒的表达式分别是是c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(OH-) 、c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3)。
OH- + H2CO3;其电荷守恒和物料守恒的表达式分别是是c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(OH-) 、c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3)。

科目:高中化学 来源:不详 题型:单选题
| A.与水反应有乙炔生成 | B.与水反应有Mg(OH)2生成 |
| C.有C-C键 | D.有C22-离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+)+c(H+)=c(OH-)+c(Cl-) |
| B.c(NH4+)+c(NH3·H2O)=2c(Cl-) |
| C.2c(OH-)—2c(H+)=c(NH4+)—c(NH3·H2O) |
| D.c(H+)=c(NH3·H2O)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
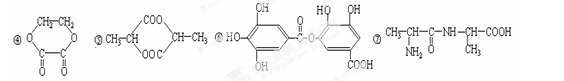
| A.①②⑤⑦ | B.②④⑤⑦ | C.②⑤⑥⑦ | D.①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)+c(H+)=c(OH+)+c(HCO3-)+c(CO32-) |
| B.2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| C.c(Na+)>c(HCO3-)>c(CO32-)>c(OH+)>c(H+) |
| D.2c(OH+)+c(CO32-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是 | A.加热 | B.加适量NaOH溶液 | C.通入氯化氢气体 | D.加入固体三氯化铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.②③④ | C.②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多 |
| B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的1/2 |
| C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7 |
| D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com