
【题目】I、煤制天然气的工艺流程简图如下:

⑴反应I:C(s) + H2O(g)![]() CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:___________________________。
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:___________________________。
⑵反应II:CO(g) + H2O(g) ![]() CO2(g) + H2(g) ΔH = 41 kJ·mol-1。如图表示不同温度条件下,煤气化反应I发生后的汽气比(水蒸气与CO物质的量之比)与CO平衡转化率的变化关系。
CO2(g) + H2(g) ΔH = 41 kJ·mol-1。如图表示不同温度条件下,煤气化反应I发生后的汽气比(水蒸气与CO物质的量之比)与CO平衡转化率的变化关系。

① 判断T1、T2和T3的大小关系:______________。(从小到大的顺序)
② 若煤气化反应I发生后的汽气比为0.8,经煤气化反应I和水气变换反应II后,得到CO与H2的物质的量之比为1:3,则反应II应选择的温度是_______(填“T1”或“T2”或“T3”)。
⑶① 甲烷化反应IV发生之前需要进行脱酸反应III。煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和_______。
② 工业上常用热碳酸钾溶液脱除H2S气体得到两种酸式盐,该反应的离子方程式是_______。
II、利用甲烷超干重整CO2技术可得到富含CO的气体,将甲烷和二氧化碳转化为可利用的化学品,其能源和环境上的双重意义重大。该技术中的化学反应为:
CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g)
2H2O(g)+4CO(g) ![]() H>0
H>0
CH4超干重整CO2的催化转化原理示意如图:

⑷过程II,实现了含氢物种与含碳物种的分离。生成H2O(g)的化学方程式是______________。
⑸假设过程I和过程II中的各步均转化完全,下列说法正确的是_______。((填序号)
a.过程I和过程II中均含有氧化还原反应
b.过程II中使用的催化剂为Fe3O4 和CaCO3
c.若过程I投料![]() ,可导致过程II中催化剂失效
,可导致过程II中催化剂失效
(6)一定条件下,向体积为2L的恒容密闭容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),发生反应CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g)
2H2O(g)+4CO(g) ![]() H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线图像如图。计算该条件下,此反应的
H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线图像如图。计算该条件下,此反应的![]() H=________________。
H=________________。

【答案】 氧气与碳发生燃烧反应放热,放出的热被可逆反应吸收利用,促进反应正向移动 T1 < T2 < T3 T3 CO2 CO32- + H2S ![]() HS - + HCO3- 4H2+Fe3O4
HS - + HCO3- 4H2+Fe3O4 ![]() 3Fe+4H2O a c +330 kJ/mol
3Fe+4H2O a c +330 kJ/mol
【解析】I、(1)C(s)+H2O(g)![]() CO(g)+H2(g)△H=+135kJmol-1,是吸热反应,而碳与氧气反应放出热量,使反应C(s)+H2O(g)
CO(g)+H2(g)△H=+135kJmol-1,是吸热反应,而碳与氧气反应放出热量,使反应C(s)+H2O(g)![]() CO(g)+H2(g),向正反应方向移动,提高碳的利用率;
CO(g)+H2(g),向正反应方向移动,提高碳的利用率;
(2)①反应CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41kJmol-1的正反应为放热反应,温度越高一氧化碳的转化率越低,由图可知,温度的大小为:T1<T2<T3;
CO2(g)+H2(g)△H=-41kJmol-1的正反应为放热反应,温度越高一氧化碳的转化率越低,由图可知,温度的大小为:T1<T2<T3;
②若煤气化反应I发生后的汽气比为0.8,设水蒸气的物质的量是4mol、则生成的CO物质的量为5mol,同时生成5mol氢气,经煤气化反应I和水气变换反应II后,设反应II中CO转化的为xmol,则生成xmol氢气,则(5-x):(5+x)=1:3,x=2.5,CO的转化率=![]() ×100%=50%,根据图知,反应温度为T3;
×100%=50%,根据图知,反应温度为T3;
(3)①根据方程式II知,生成的酸性气体还有二氧化碳;
②工业上常用热碳酸钾法脱除H2S气体得到两种酸式盐,则二者反应生成碳酸氢钾和硫氢化钾,反应方程式为K2CO3+H2S═KHS+KHCO3;
II、⑷由图示可知,过程II中氢气还原Fe3O4生成H2O,发生反应的化学方程式是4H2+Fe3O4 ![]() 3Fe+4H2O;
3Fe+4H2O;
⑸假设过程I和过程II中的各步均转化完全,下列说法正确的是_______。((填序号)
a.过程I有氢气生成,而过程II中存在氢气还原四氧化三铁和CO还原四氧化三铁,均属于氧化还原反应,故a正确;b.过程II中使用的催化剂为Fe3O4和CaO,故b错误;c.若过程I投料![]() ,则CH4和CO2恰好生成CO和H2,无多余的CO2,导致过程II中只能生成FeO,催化剂效果降低,故c正确;答案为ac;
,则CH4和CO2恰好生成CO和H2,无多余的CO2,导致过程II中只能生成FeO,催化剂效果降低,故c正确;答案为ac;
(6) CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)
起始物质的量(mol) 1.2 4.8 0 0
变化物质的量(mol) x 3x 2x 4x
平衡物质的量(mol) 1.2- x 4.8-3x 2x 4x
平衡时CH4的体积为![]() =
=![]() ,解得x=0.36mol,则
,解得x=0.36mol,则![]() H=+118.8×
H=+118.8×![]() kJ/mol=+330kJ/mol。
kJ/mol=+330kJ/mol。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下图为铜锌原电池的装置图,根据装置图填写空白.
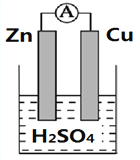
(1)将________转化为________的装置叫做原电池
(2)Zn极上的电极反应式为:_____________________________________。
(3)Cu极发生的是_____________反应(“氧化”或“还原”)。铜片上观察到的现象为___________________;
(4)溶液中H+的流动方向为__________________;
(5)若烧杯中溶液为AgNO3溶液,则负极为________(填Zn或Cu),总反应方程式为________________________________。
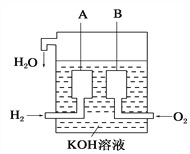
(6)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应物为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 原电池的正极材料必须是金属
B. 原电池的负极发生还原反应
C. 实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
D. 原电池可以把物质内部的能量全部转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

⑴ 该反应的化学方程式为:_________________________
⑵ 反应开始至2min,用Z表示的平均反应速率为:_____________
⑶ 下列叙述能说明上述反应达到化学平衡状态的是_____(填序号)
A.混合气体的总压强不随时间的变化而变化
B.混合气体的平均摩尔质量不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的总质量不随时间的变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国卫生部门制定的《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”。香烟燃烧产生的烟气中,有多种有害物质,其中尼古丁(C10H14N2)对人体危害最大,下列说法正确的是
A.尼古丁是由26个原子构成的物质
B.尼古丁中C、H、O 三种元素的质量比为10:14:2
C.尼古丁的相对分子质量是162g
D.尼古丁中氮元素的质量分数为17.3 %
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_____________;
(2)写出氮气分子的结构式____________。
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。
含有极性键和非极性键的是_______;
含有非极性键的离子化合物是_____。(填序号,下同)
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦碘升华;⑧溴蒸气被木炭吸附。
(1)未破坏化学键的是_____________;
(2)仅离子键被破坏的是_____________;
(3)仅共价键被破坏的是_____________。
Ⅳ.下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④14N、14C
(1)互为同位素的是:______;
(2)互为同素异形体的是:______;
氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种光致抗蚀剂,可用于印刷电路和集成电路工艺中,其合成路线如下:
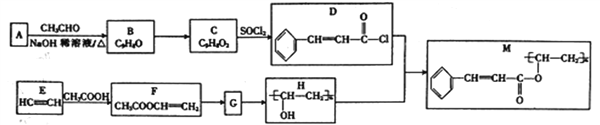
已知:I. 
II.羟基直接连接在碳碳双键的碳原子上的有机物是不稳定的。
回答下列问题:
(1)下列关于M的说法正确的是______(填字母)。
a.M属于高分子化合物
b.M在碱性溶液中能稳定存在
c.M能使酸性高锰酸钾溶液褪色
d.1molM与足量氢气反应时,最多消耗4molH2
(2)C中官能团的名称为______,由E生成F的反应类型为_________。
(3)F的化学名称为_______,由F生成G的化学方程式为____________。
(4)二取代芳香族化合物W(只含苯环,不含其他的环,且不含“C=C=C”结构)是D的同分异构体,W能与三氯化铁溶液发生显色反应,则W的结构共有____种(不含立体异构),其中核磁共振氢谱为五组峰的结构简式为____________。
(5)参照上述合成路线,设计一条以HC≡CH为原料(其他无机试剂任选)制备G的合成路线:________________________。
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com