
【题目】将标准状况下的HCl气体4.48 L溶于水形成100 mL溶液,然后与足量的铁屑充分反应。计算:
(1)所得盐酸溶液的物质的量浓度_______________
(2)参加反应的铁的质量____________
(3)生成的H2的体积(标况)___________
(4)将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度____________
【答案】2.0mol/L 5.6g 2.24L 0.25mol/L
【解析】
(1)4.48LHCl气体的物质的量=![]() ,HCl溶于水所得盐酸的物质的量浓度为
,HCl溶于水所得盐酸的物质的量浓度为![]() 。
。
(2)设参加反应的铁的质量为m(Fe),根据方程式计算:
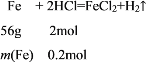
列比例式:![]() ,解得m(Fe)=5.6g,所以参加反应的铁的质量为5.6g。
,解得m(Fe)=5.6g,所以参加反应的铁的质量为5.6g。
(3)设生成的H2的体积(标准状况)为V(H2),根据方程式计算:
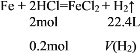
列比例式:![]() ,解得V(H2)=2.24L,即生成的H2的体积为2.24L。
,解得V(H2)=2.24L,即生成的H2的体积为2.24L。
(4)设生成的FeCl2的物质的量为n(FeCl2),根据方程式计算:
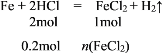
列比例式:![]() ,解得n(FeCl2)=0.1mol,将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度
,解得n(FeCl2)=0.1mol,将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知烃D在标准状况下的密度为1.25g·L-1,C、H都是具有浓郁香味、不易溶于水的油状液体。相关物质转化关系如下(转化条件都已省略):
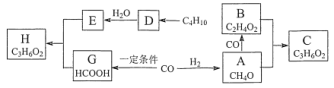
请回答:
(1)B中官能团的名称是____。
(2)C4H10→D的反应条件是____。
(3)E+G→F的化学方程式____。
(4)下列说法正确的是____。
A. C、H属于同一种物质
B. 可以用新制氢氧化铜悬浊液鉴别B、E和G
C. 有机物A、G在一定条件下反应所得产物是B的同分异构体
D. 一定条件下A转化成G,B转化成E,都属于氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型锂-空气电池其工作原理如图所示。放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
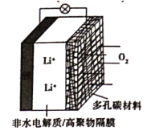
A.锂电极为正极
B.外电路电子由多孔碳材料电极流向锂电极
C.多孔碳材料的O2失电子转化为O2-
D.电池总反应为2Li+(1-x/2)O2=Li2O2-x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:形成KBr晶体时的能量变化如图所示,下列说法正确的是
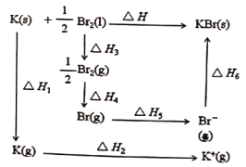
A.△H1<0,△H2<0
B.△H3-△H4<0
C.△H6=△H3+△H4+△H5-△H
D.△H=△H1+△H2-△H3-△H4-△H5-△H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从该溶液中取出10 mL,含NaOH的质量为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成一种药物的中间体,可通过以下方法合成:
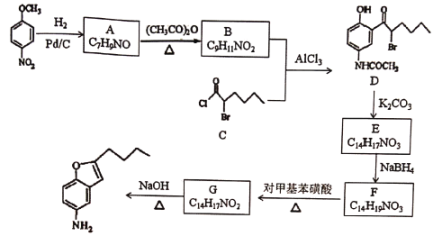
已知:①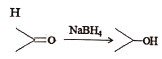 ②
②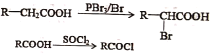
(1)化合物F的结构简式_____。
(2)下列说法正确的是_____。
A. 由反应物转化为A,E转化为F均发生了还原反应
B. 化合物F中有2个手性碳原子
C. 1molG能与5molH2发生加成反应
D.化合物H的分子式为C12H15NO
(3)写出D→E的化学方程式______。
(4)请写出以正己醇为原料制备化合物C的流程图,无机试剂任选。________________
(5)写出同时满足下列条件的B的所有同分异构体的结构简式______。①分子中只有4种不同化学环境的氢②分子中不含氮氧键、C=O③分子中只有一个环状结构,且遇FeCl3溶液显紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】色香味俱佳、口感好的食品深受人们的喜爱。为了提高食品的质量,在生产过程中往往会加入一些能改变食品某些性质的物质。请按照题意要求填空:
(1)某课外小组学生学做比萨饼, 购买了下列食物:①西红柿、②食盐、③橄榄油④小麦粉.请回答:
其中富含淀粉的是________(填序号,下同),富含油脂的是________,富含维生素的是________,属于调味剂的是________;
(2)味精是常用的一种鲜味剂,其有效成分是谷氨酸钠,它的结构简式如下图,该物质分子中所含的官能团有________和________ (填写名称); 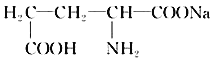
(3)碳酸氢钠是常见的疏松剂,主要是因为它在加热条件下产生了气体,使食品变得疏松。试写出碳酸氢钠受热分解的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中,充入2molCO2和6molH2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
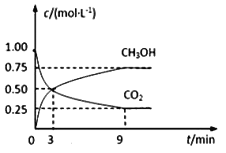
(1)0~9min内,v(H2)=__mol·L1·min1。
(2)能说明上述反应达到平衡状态的是__(填编号)。
a.反应中CO2与CH3OH的物质的量浓度之比为1:1
b.混合气体的密度不随时间的变化而变化
c.单位时间内消耗3 mol H2,同时生成1 mol H2O
d.CO2的体积分数在混合气体中保持不变
e.混合气体的压强不随时间的变化而变化
(3)平衡时H2的转化率为___。
(4)平衡时混合气体中H2O(g)的体积分数是__。
(5)一定温度下,第9分钟时v正(CH3OH)__(填“大于”、“小于”或“等于”)第3分钟时v逆 (CH3OH)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com