
【题目】下列氧化还原反应中,电子转移的方向和数目均正确的是( )
A.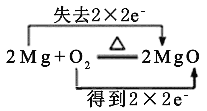
B.
C.
D.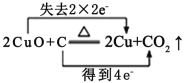
【答案】A
【解析】
A. Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4;
B.反应中Cl元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为12;
C. 氧化还原反应中得失电子数应该相等;
D. CuO与C反应中,铜得电子,C失电子。
A. Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4,则电子转移的方向和数目为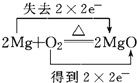 ,A项正确;
,A项正确;
B. 该反应中Cl元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为12,则电子转移的方向和数目为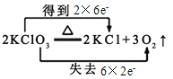 ,B项错误;
,B项错误;
C. 氧化还原反应中得失电子数应该相等,则碳与氧气反应时,电子转移的方向和数目为 ,C项错误;
,C项错误;
D. CuO与C反应,铜得电子,C失电子,则电子转移的方向和数目为 ,D项错误;
,D项错误;
答案选A。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)![]() Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
A. 反应容器中压强不再变化 B. 混合气体的密度不再变化
C. 混合气体的平均相对分子质量不再变化 D. Z的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用乙醇、乙酸和浓硫酸制备乙酸乙酯,分别设计了甲、乙两套装置。按图连接好装置,添加试剂后用酒精灯对左边试管小火加热3~5min后,改用大火加热,当观察到右边试管中有明显现象时停止实验。已知:乙酸乙酯的沸点为77°C,乙醇的沸点为78.5°C,乙酸的沸点为117.9°C。

(1)写出甲装置左边试管中主要发生的反应的化学方程式:______。
(2)加入的浓硫酸作用为____,装置乙中球形干燥管的作用是_____。
(3)反应开始时用酒精灯对左边试管小火加热的原因是________。
(4)停止加热后,振荡a、b两试管发现油状液体层变薄,其主要原因可能是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关碱金属铷(Rb)的叙述中,正确的是( )
A. 灼烧氯化铷时,火焰有特殊颜色B. 硝酸铷是共价化合物,易溶于水
C. 在钠、钾、铷三种单质中,钠的金属性最强D. 氢氧化铷是弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种变化是因为构成原电池的是( )
A.在空气中金属铝表面迅速氧化形成保护层
B.金属表面涂漆以阻止金属被氧化
C.红热的铁丝与水接触铁表面形成黑色物质
D.铁与稀硫酸反应时,加人少量硫酸铜溶液后可使反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
K为化学平衡常数,其中K和温度的关系如下表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是
A. 此反应为放热反应
B. 此反应只有达到平衡时,密闭容器中的压强才不会变化
C. 此反应达到1 000℃时的反应速率比700℃时大
D. 该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是合成尼龙66的重要原料。以环己烯为原料,可以与多种氧化剂反应得到己二酸(反应均在一定条件下进行)。下列氧化剂中可以称为绿色化学试剂的是( )
A.高锰酸钾B.过氧化氢C.硝酸D.重铬酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的电离平衡曲线如图所示,试回答下列问题:

(1)图中ABCDE五点的KW间的大小关系是___________.(用ABCDE表示)
(2)若从A点到D点,可采用的措施是______.
a.升温
b.加入少量的盐酸
c.加入少量的NaOH固体
(3)点B对应温度条件下,某溶液pH═7,此时,溶液呈____(酸性、碱性、中性),点E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________.
(4)点B对应的温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是pH1+ pH2= ___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5时,发生以下两个分解反应:N2O5![]() N2O3+O2,N2O3
N2O3+O2,N2O3![]() N2O+O2,在1 L密闭容器中加热4 mol N2O5达到化学平衡时c(O2)为4.50 mol/L,c(N2O3)为1.62 mol/L,则在该温度下各物质的平衡浓度正确的是
N2O+O2,在1 L密闭容器中加热4 mol N2O5达到化学平衡时c(O2)为4.50 mol/L,c(N2O3)为1.62 mol/L,则在该温度下各物质的平衡浓度正确的是
A. c(N2O5)=1.44 mol/L B. c(N2O5)=0.94 mol/L
C. c(N2O)=1.40 mol/L D. c(N2O)=3.48 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com