
【题目】已知水的电离平衡曲线如图所示,试回答下列问题:

(1)图中ABCDE五点的KW间的大小关系是___________.(用ABCDE表示)
(2)若从A点到D点,可采用的措施是______.
a.升温
b.加入少量的盐酸
c.加入少量的NaOH固体
(3)点B对应温度条件下,某溶液pH═7,此时,溶液呈____(酸性、碱性、中性),点E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________.
(4)点B对应的温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是pH1+ pH2= ___________.
【答案】B>C>A=D=E b 碱性 10:1 14
【解析】
(1)Kw只与温度有关,温度升高促进水的电离,据此分析;
(2)仔细观察图像,溶液由A点中性转化为D点酸性,据此分析;
(3)25℃时所得混合溶液的pH=7,酸碱恰好中和,即n(OH-)=n(H+),据此分析;
(4)温度为100℃,水的离子积为10-12,由于反应后溶液呈中性,所以n(OH-)=n(H+),据此分析。
(1)Kw只与温度有关,温度升高促进水的电离,Kw增大,因此有B>C>A=D=E;综上所述,本题答案是:B>C>A=D=E。
(2)从A点到D点,溶液由中性转化为酸性,因此选项b与题意相符;综上所述,本题选b。
(3)点B对应温度为100℃,Kw=10-12,pH=6,溶液为中性;温度不变时,某溶液pH=7,此时,溶液呈碱性;点E对应温度为25℃,Kw=10-14,25℃时所得混合溶液的pH=7,酸碱恰好中和,即n(OH-)=n(H+),则V(NaOH)×10-5mol/L=V(H2SO4)×10-4mol/L,得V(NaOH):V(H2SO4)=10:1;综上所述,本题答案是:碱性,10:1。
(4)点B对应的温度为100℃,水的离子积常数为10-12,pH=b的某强碱溶液中c(OH-)=10b-12,反应后溶液呈中性,所以n(OH-)=n(H+),即100×10-a=1×10b-12,故a+b=14,即pH1+pH2=14;综上所述,本题答案是:14。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重。目前,世界各国已高度重视这个问题,并采取积极措施进行治理。
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法都正确的是__________(填字母编号,可多选)。

(2)下图是某市污水处理的工艺流程示意图:

①下列物质中不可以作为混凝剂(沉降剂)使用的是______(填字母编号,可多选)。
A.偏铝酸钠 B.氧化铝
C.碱式氯化铝 D.氯化铁
②混凝剂除去悬浮物质的过程是________(填字母编号)。
A.物理变化 B.化学变化
C既有物理变化又有化学变化
(3)在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
某厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2===KOCN+2KCl+H2O再投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:
___KOCN+___KOH+___Cl2―→___CO2+___N2+___KCl+___H2O。若处理上述废水20 L,使KCN完全转化为无毒物质,至少需液氯__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中不正确的是( )
A. 盐酸滴在石灰石上:CaCO3+2H+![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
B. 向Ba(OH)2溶液中滴入少量的NaHSO4溶液:H++SO42-+Ba2++OH-![]() BaSO4↓+H2O
BaSO4↓+H2O
C. 向Ba(OH)2溶液中滴入过量的NaHSO4溶液:2H++SO42-+Ba2++2OH-![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 稀硫酸滴在铜片上:Cu+2H+![]() Cu2++H2↑
Cu2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法不正确的是
)是其中的一种。下列关于该化合物的说法不正确的是
A. 与环庚烯互为同分异构体 B. 二氯代物共有6种(不含立体异构)
C. 所有碳原子不可能处在同一平面 D. 1mol该化合物含有20mol共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌浮渣主要含Zn、ZnO、SiO2、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超细活性氧化锌,其工艺流程如下:
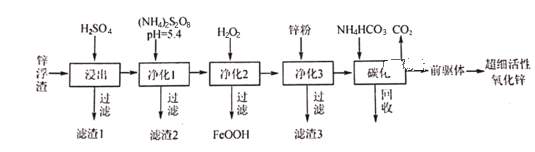
(1)滤渣1的成分为___________。
(2)在S2O82-的结构式中只含有一根“O一O”非极性键,则S的化合价为___________;工业上常用惰性电极电解(NH4)2SO4生产(NH4)2S2O8(过二硫酸铵),阳极电极反应式为__________________。净化1是为了将Mn2+转化为MnO2而除去,写出该反应的离子方程式:______________________。
(3)净化3的目的_________________________________。
(4)碳化回收溶液的主要成分为___________,该物质循环使用的目的___________________。
(5)碳化在50℃进行,“前驱体”的化学式为ZnCO3·2Zn(OH)2·H2O,写出碳化过程生成“前驱体”的化学方程式:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对氧化还原反应的分析中合理的是( )
A. Mg变成MgO时化合价升高,失去电子,因此Mg在该反应中被还原了
B. KMnO4受热分解,Mn元素化合价一方面升高,一方面降低,因此Mn元素既被氧化又被还原
C. CuSO4+2NaOH=Cu(OH)2↓+Na2SO4不属于氧化还原反应
D. 反应2H2O![]() 2H2↑+O2↑,H2O中H元素的化合价既有升高,又有降低
2H2↑+O2↑,H2O中H元素的化合价既有升高,又有降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1。一定条件下,向1 L密闭容器中投入0.8 mol的NH3和1.6 mol的O2,发生上述反应,第2 min和第4 min时NH3的物质的量分别为0.6 mol和0.3 mol。下列说法中不正确的是
A. 上述反应的逆反应的活化能不小于905.9 kJ·mol-1
B. 反应在第2 min到第4 min时,O2的平均速率为0.15 mol·L-1·min-1
C. 反应第2 min时改变了某一条件,该条件可能是使用催化剂或升高温度
D. 平衡后降低压强,混合气体平均摩尔质量减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com