
 ;
;  .
.


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
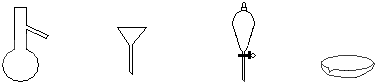
| A、蒸馏、蒸发、萃取、过滤 |
| B、过滤、蒸发、萃取、蒸馏 |
| C、萃取、过滤、蒸馏、蒸发 |
| D、蒸馏、过滤、萃取、蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两溶液中水的电离度比较:②>① |
| B、分别加入少量NaOH固体,恢复到原温度,c(CO32-)均增大 |
| C、①溶液中:c(CO32-)<c(H2CO3) |
| D、②溶液中:c(HCO3-)<c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位时间内减少n mol A2,同时生成2n mol AB |
| B、单位时间内生成n mol B2,同时生成n mol AB |
| C、单位时间内生成 2xmol AB,同时生成xmol A2 |
| D、容器内各组成成分的物质的量之和不随时间变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
| 实验 编号 | 铜片 质量/g | 0.1mol?L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 实验①和②探究 |
| ② | 5 | 20 | 0.5 | 0 | |
| ③ | 5 | 20 | 0 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铜片放入稀硫酸中,无现象.若再向所得的溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 |
| B、在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| C、将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 |
| D、两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,等体积的CH4和CO2所含共用电子对数相等 |
| B、与NaOH溶液、H2SO4溶液反应产生等量H2,所需铝粉质量相等 |
| C、1 mol OH-和17 g NH3所含电子数相等 |
| D、明矾溶液中K+和Al3+物质的量浓度相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com