
����Ŀ���Ͼ���ʾ�������к�SiO2��Fe2O3��CeO2��FeO�����ʡ�ij����С���Դ˲�����ĩΪԭ�ϣ��Ƶ�Ce(OH)4��������立���Fe2(SO4) 3��(NH4) 2SO4��24H2O�ݣ��������������
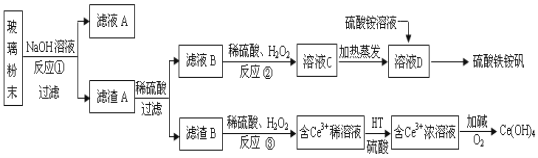
��֪�������������£�����ˮ��Һ����Ce3+��Ce4+������Ҫ������ʽ��Ce4+�н�ǿ�����ԣ���CeO2������ϡ���ᣬҲ������NaOH��Һ��
�ش��������⣺
(1)��Ӧ�������ӷ���ʽ�� ��
(2)��Ӧ����H2O2�������� ��
(3)��Ӧ�������ӷ���ʽ�� ��
(4)��֪�л���HT�ܽ�Ce3+��ˮ��Һ����ȡ�������ù��̿ɱ�ʾΪ��
2Ce3+ (ˮ��)+ 6HT(�л���)![]() 2CeT3 (�л���)+ 6H+(ˮ��)
2CeT3 (�л���)+ 6H+(ˮ��)
��ƽ��ǶȽ��ͣ���CeT3 (�л���)����H2SO4 ��ýϴ��ĺ�Ce3+��ˮ��Һ��ԭ���� ��
(5)������立���Fe2(SO4) 3��(NH4) 2SO4��24H2O�ݹ㷺����ˮ�ľ����������侻ˮԭ�������ӷ���ʽ������ ��
���𰸡�(1)SiO2 + 2OH- = SiO32- + H2O(2��)
(2)����ʹFe2+ת��ΪFe3+(2��)
(3)2GeO2 + 6H+ + H2O2 = 2Ge3+ + 4H2O + O2��(2��)
(4)���Һ�м���H2SO4ʹc(H+)������ƽ�����γ�Ge3+ˮ��Һ�����ƶ���(2��)
(5)Fe3+ + 3H2O![]() Fe(OH)3(����) + 3H+ (2��)
Fe(OH)3(����) + 3H+ (2��)
��������
����������ϲ�����ĩ������������Һ�������������������Ʒ�Ӧ���ɹ����ƺ�ˮ�����ˣ��õ�����A�ijɷ���Fe2O3��CeO2��FeO������A��Fe2O3��CeO2��FeO����ϡ�������˵���ҺB������������Һ��������������������������������ҺC��Ϊ�������������������������ⲻ���������ʣ����������õ���ҺDΪ������������Һ������Һ�м����������Һ�õ�������立�������B�ijɷ���CeO2��CeO2��H2O2��ϡH2SO4��Ӧ����Ce3+��O2������HT������ȡ����Ce3+��ˮ��Һ����ȡ������Ce3+�Ӽ����������������ԭ��Ӧ����Ce��OH��4��
��1���������Ϸ�����֪��Ӧ�������ӷ���ʽΪSiO2 + 2OH- = SiO32- + H2O��
��2����Ӧ����H2O2������������ʹ��������Ϊ��������
��3����Ӧ����������Һ��CeO2���������ԭ����Ce3+���ӣ��������ⱻ����������������Ӧ�����ӷ���ʽ2GeO2+6H++H2O2=2Ge3++4H2O+O2����
��4���л���HT�ܽ�Ce3+��ˮ��Һ����ȡ�������ù��̿ɱ�ʾΪ��2Ce3+��ˮ�㣩+6HT���л��㣩�T2CeT3���л��㣩+6H+��ˮ�㣩��������������������Ũ�ȣ�ƽ������������γ�Ge3+ˮ��Һ�����ƶ�����ýϴ��ĺ�Ce3+��ˮ��Һ��
��5��������立�[Fe2��SO4��3��NH4��2SO424H2O]�㷺����ˮ�ľ����������侻ˮԭ�����ܽ����Һ�е�������ˮ�����������������壬������������������ʵ����ã����Ծ�ˮ����Ӧ�����ӷ���ʽΪ��Fe3++3H2O![]() Fe��OH��3+3H+��
Fe��OH��3+3H+��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A������ȼ�ջ�ʯȼ�������������һ����Ҫ����
B��ʳƷ�еĿ���������������������������
C����SO42���ij�����Һ�в��ẬBa2+
D��������ˮ�ܵ����H+���ӵĻ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ֱ����������£�п���϶�ͭʱ������ͭ���� ��
A������ B������ C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������X��Y��Z��M��N�����ǵ������ӿ�����SO![]() ��Cl����NO
��Cl����NO![]() ��CO
��CO![]() �������ӿ�����Ag����NH
�������ӿ�����Ag����NH![]() ��Na����Al3����Cu2����Ba2����Fe3������֪��
��Na����Al3����Cu2����Ba2����Fe3������֪��
��M����ɫ��Ӧ�ʻ�ɫ��
�������ξ�����ˮ��ˮ��Һ��Ϊ��ɫ��
��X����Һ�����ԣ�Y��Z��N����Һ�����ԣ�M����Һ�ʼ��ԡ�
�������������ε���Һ�зֱ����Ba(NO3)2��Һ��ֻ��X��Z����Һ������������
�������������ε���Һ�У��ֱ���백ˮ��N��Z����Һ�����ɳ����������Ӱ�ˮ��Z�г�����ʧ��
�ް�X����Һ�ֱ���뵽Y��Z��N����Һ�У��������ɲ�����ϡ����ij�����
��ش��������⣺
(1)�������У�������������ͬ�������εĻ�ѧʽ��__________________
(2)M��Һ�Լ��Ե�ԭ����(�����ӷ���ʽ��ʾ)______________________
(3)X��Z����Һ��Ӧ�����ӷ���ʽ��_______________________
(4)N�Ͱ�ˮ��Ӧ�����ӷ���ʽ��___________________________
(5)��Ҫ����Y�������������ӣ���ȷ��ʵ�鷽����____________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��С��ͬѧ����һ����ij��ֽ���۳���Ư��Һ(NaCl��NaClO�Ļ��Һ)����ʢ�ű���KAl(SO4)2��Һ�ij��У�����ж��¼�����С��ͬѧΪ̽���ж�ԭ�����������ʵ�顣
(1)С��ͬѧ����Ư��Һ����Ư�������������Ʋ⣬Ư��Һ��ClO�����������ԡ�ʵ�����£�
��. ��pH��ֽ���飬Ư��ҺpH>7������![]() ��ҺpH<7��
��ҺpH<7��
��. ȡ10 mLƯ��Һ�����μ���Na2SO3��Һ��BaCl2��Һ���а�ɫ�������ɣ��������ɫ�������������ᡣ
��. ��ȡ10 mL��Ư��Һ������Ʒ����Һ����Һ��ɫ��dz��һ��ʱ�����Ϊ��ɫ��
��. ��ȡ10 mLƯ��Һ������Ʒ����Һ����������ϡ�����ữ����Һ��ɫ������Ϊ��ɫ��
��Ư��ҺpH����7��ԭ����(�����ӷ���ʽ��ʾ)__________��
����ʵ���ó�ClO�����������ԣ�д����Ӧ�����ӷ���ʽ__________��
�۶Ա�ʵ���͢�˵��ClO������������Һ����ԵĹ�ϵ��__________��
(2)С��ͬѧ����(1)�е�ʵ�飬�����Ư��Һ��������Һ����Cl2���ɡ���ͼ��ʾ��װ�ü���ʵ�飬̽��Ư��Һ��������Һ���Ƿ��ܷ�Ӧ����Cl2��
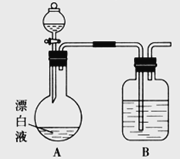
��װ��B��������__________��ʢ�ŵ�ҩƷ��__________��
������Һ©����������ƿ�м������ᣬ������ƿ���л���ɫ���������A�з�Ӧ�����ӷ���ʽ________��
������Һ©����������ƿ�м��뱥��![]() ��Һ���۲쵽���������İ�ɫ��״������ͬʱ�л���ɫ���������A�м�
��Һ���۲쵽���������İ�ɫ��״������ͬʱ�л���ɫ���������A�м�![]() ��Һ��Ӧ�����ӷ���ʽ��__________��
��Һ��Ӧ�����ӷ���ʽ��__________��
(3)����ʵ��˵��Ư��Һ��������Һ��ϻ����Cl2����ȡ10 mLƯ��Һ������BaCl2��Һ��Ϻ���ͨ��SO2����������ʵ������п��ܵ�ʵ��������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ȷ������ ��
A������ʽ����CnH2n��2����һ��������
B��������������ˮ����ȡ����Ӧ
C����������۷е������ĸ�
D���������ܱ����Ը�����ص�ǿ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȵ�ԭ������Ϊ17��37Cl��35Cl���ȵ�����ͬλ�أ�����˵����ȷ���ǣ���
A. 35Clԭ������������Ϊ18
B. ![]() mol��H35Cl��������������ԼΪ6.02��1023
mol��H35Cl��������������ԼΪ6.02��1023
C. 3.5 g��35Cl2��������Ϊ2.24 L
D. 35Cl2�����Ħ������Ϊ70
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Һ��ɵ�������������
A����ɫ��Һ�п��ܴ�������Al3+��NH4+��Cl��S 2-
B��������Һ�п��ܴ�������Na+��ClO��SO42-��I
C����������Һ�п��ܴ�������Na+��K+��Cl��HCO3
D��������Һ�п��ܴ�������Fe3+��K+��Cl��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ�û�����ܴﵽʵ��Ŀ�ĵ���

A. ͼ1װ�������к��ȵIJⶨ
B. ͼ2װ�����ڲⶨ�����ķ�Ӧ���ʣ���λmL/s��
C. ͼ3װ�������о�����Cu2+��Fe3+�Է�Ӧ���ʵ�Ӱ��
D. ͼ4װ��������֪Ũ�ȵĸ��������Һ�ⶨδ֪Ũ�ȵIJ�����Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com